| Головна |
| «« | ЗМІСТ | »» |
|---|
Епідеміологія, етіологія і патогенез. Рак шлунка - друга за частотою причина смерті від злоякісних новоутворень у світі. Щорічно на земній кулі захворює понад 1 млн осіб. Найвища захворюваність зареєстрована в Японії (78 випадків па 100 тис. Населення), деяких країнах Центральної Європи, Скандинавії, колишнього СРСР. У Росії ця патологія зустрічається з частотою 40 хворих на 100 тис. Населення, в Японії - 59, Фінляндії - 49, США - 7,2.
У Росії рак шлунка займає друге місце в структурі онкологічної захворюваності, поступаючись лише раку легенів у чоловіків і раку молочної залози у жінок. Захворюваність становить у чоловіків - 29,5 випадку на 100 тис. Населення, у жінок - 12,6. У нашій країні питома вага раку шлунка в структурі всіх онкологічних захворювань складає 12,3%, а смертності - 16,3%.
До етіологічних чинників раку шлунка відносять різноманітну групу речовин, хімічних сполук, звану канцерогенами, серед яких виділяють канцерогени екзогенні та ендогенні. Встановлено, що абсолютних канцерогенів не існує.
Відомо, що в регіонах з кислою, багатою органічними речовинами грунтом відзначається збільшення показників захворюваності. До етіологічних чинників, що робить вплив на виникнення раку шлунка в промисловій сфері, відносять виробництво гуми, азбесту, полівінілхлориду, мінеральних масел, хрому і т. Д. Остаточно не вивчено вплив іонізуючого випромінювання на розвиток раку шлунка, проте високий рівень радіаційного фону та вміст радіонуклідів в їжі і воді вважаються факторами ризику.
Оскільки слизова оболонка шлунка постійно піддається контакту з їжею, значне місце в гіпотезах про етіологію раку шлунка відводять аліментарних чинників, зловживання алкоголем і куріння. Цілком очевидно, що на величину показника захворюваності населення на рак шлунка впливає характер і режим харчування. Наявність в раціоні достатньої кількості рослинної злиденні і фруктів, мікроелементів і вітамінів, зокрема вітамінів А, Е і С, тварин і рослинних білків істотно знижує ризик виникнення раку шлунка. Найбільш наочний в цьому приклад - США, де за останні 70 років пропаганди раціонального харчування багаторазово знизилася захворюваність населення на рак шлунка.
В останні роки особливе значення в канцерогенезі відводять деяких хімічних речовин. Найбільш активні з них - N-ішпрозосоедііеіія. Експериментально доведено, що додавання в їжу нітрозосоедіне- ний в 90% спостережень викликає у лабораторних мишей розвиток раку шлунка. Синтез в шлунку людини канцерогенних сполук, що надходять з убогої і водою, може відбуватися як в кислому, так і в слабокислою і нейтральному середовищі.
В даний час все більше уваги приділяють впливу Helicobacter pylori на виникнення раку шлунка. Це обумовлено повідомленнями вітчизняних та зарубіжних дослідників, які відзначають збільшення рівня захворюваності в осіб, інфікованих даними мікроорганізмом.
У США і Англії дослідження показали, що ризик виникнення раку шлунка у інфікованих пацієнтів в 3,8 рази вище в порівнянні з неінфікованими хворими. За класифікацією Всесвітньої організації охорони здоров'я (ВООЗ) Helicobacter pylori відноситься до групи I (явні канцерогени).
У 1975 р на підставі вивчення різноманітних епідеміологічних даних П. Корреа сформулював патогенетичну модель раку шлунка. Суть її полягає в тому, що протягом значного проміжку часу надмірне споживання солі та інших дратують слизову оболонку харчових чинників призводить до руйнування захисного слизового бар'єру, гострого запалення, некрозу, що повторюється регенерації слизової оболонки. Цьому ж може сприяти рефлюкс дуоденального вмісту в шлунок. Також слід зазначити роль аутоімунних процесів з пошкодженням головних і обкладочнихклітин.
Повторювані дії цих факторів поряд з надходженням і синтезом нитрозосоединений призводять до формування хронічного гастриту з нерівномірною атрофією спеціалізованих залоз. У переважній більшості випадків ці зміни не супроводжуються клінічними проявами захворювання. Крім атрофічні зміни залоз з'являється кишкова метаплазія, яку можна розглядати як неспецифічну приспособительную або регенераторні реакцію епітелію. Поява цих змін може призводити до зниження шлункової секреції: спочатку соляної кислоти, потім пепсину. Недостатнє надходження речовин, що знижують ефективність реакції нітрозірова- ня аминосоединений, особливо вітамінів А, С і Еу а також імунодепресія в цих умовах забезпечують канцерогенний вплив нитро- зосоедіненій, поява і поступове наростання атипових реакцій з переходом в преінвазивний і далі інвазивний рак.
ВООЗ визнала, що з морфологічної точки зору передрак існує, причому слід розрізняти передракові стани і передракові зміни.
передраковий, або фонове, стан - поняття клінічне і включає в себе ті захворювання шлунка, які найбільш часто передують розвитку раку. Передракові зміни - це сума морфологічних ознак, які називаються дисплазією, що передують і супутніх раку.
дисплазія - поняття, яке включає в себе клітинну атипию, порушення диференціації і структури слизової оболонки. У більшості випадків слабка і помірна дисплазія має зворотний розвиток або залишається стабільною, хоча безсумнівна можливість її трансформації в рак. Важка ступінь дисплазії також здатна піддаватися зворотному розвитку, однак імовірність її виникнення злоякісної пухлини досить велика і може досягати 75%.
Морфологічні дослідження встановили, що основним передракових захворюванням при початковому раку шлунка служить хронічний гастрит (Близько 90%), в тому числі і в оперованоюшлунку. Менш значимі аденоми (до 8-10%), гіперпластичні поліпи (близько 3%), виразка шлунка (до 1-2%).
До ранньої онкологічної патології шлунка відносяться передракові зміни слизової оболонки, рак in situ і інвазивний рак (пухлина діаметром до 1 см, яка не проростає в підслизовий шар).
Фахівці Японського товариства гастроентерологів-ендосконістов терміном «ранній» запропонували визначати рак, розташований в межах слизової оболонки шлунка без проникнення в підслизовий шар, незалежно від наявності або відсутності метастазів в лімфатичні вузли.
За даними японських авторів, при розташуванні раку шлунка в межах слизової оболонки 5-річна виживаність хворих після радикальної операції досягає 100%; при проростанні пухлини в підслизовий шар цей показник знижується до 75%; при інвазії раку в м'язову і серозну оболонки шлунка 5-лстняя виживаність становить нс більше 25%.
Поєднання передракових станів з передраковими змінами підвищує ризик розвитку раку шлунка.
До передракових захворювань, на основі яких може розвинутися рак шлунка, відносять: хронічний атрофічний і гіпертрофічний гастрит, ригідний антральний гастрит, виразкову хворобу шлунка, поліпи і поліпоз шлунка, хвороба Менетріє (складчастий гастрит), пернициозную анемію, атрофічний гастрит кукси шлунка.
Частота малігнізації виразки шлунка, але даними більшості авторів, коливається від 1 до 17%. Як передракових розглядають частіше каллезной виразку, хоча правильніше розцінювати кожну виразку шлунка (будь-яких розмірів) як потенційно злоякісну.
Більшість дослідників рекомендують в якості диференційно-діагностичного прийому проводити курс противиразкової терапії протягом
4-6 тижнів. Якщо виразка шлунка протягом зазначеного строку не рубцюється, необхідно пропонувати пацієнтам операцію. Разом з гем необхідно пам'ятати, що і невеликі ракові виразки можуть тимчасово епітелізіровалісь під дією противиразкових препаратів.
Менш значимі в структурі початкового раку шлунка малігнізованих поліпи, при цьому потенціал малігнізації у різних типів поліпів неоднаковий: аденоми (аденоматозні поліпи) озлокачествляются в 36%, а гіперпластичні - в 3,5% випадків.
У хворих пернициозной анемією (обумовленою недостатністю в організмі вітаміну BV1) постійно спостерігається хронічний атрофічний гастрит. У багатьох випадках він протікає з кишковою метаплазією епітелію шлунка. Рак шлунка при перніциозної анемії зустрічається в 3-5 разів частіше, ніж у здорових людей.
Хвороба Мснетріе - своєрідне і дуже рідкісне захворювання шлунка, яке характеризується гіперплазією епітелію і різким потовщенням складок слизової оболонки. Клінічна картина при цьому характеризується болями в епігастральній ділянці, схудненням і нудотою. Захворювання має хронічний перебіг. Іноді спостерігається спонтанне одужання або перехід в хронічний атрофічний гастрит. Рак виникає приблизно у 10% хворих.
Хронічний гастрит кукси шлунка нерідко супроводжується дисплазією і кишковою метаплазією епітелію. Патологічні зміни з плином часу прогресують, частота їх зростає. Створюються умови для виникнення раку кукси шлунка.
Рак кукси шлунка виникає у 2-6% з числа оперованих з приводу доброякісних захворювань шлунка. Чоловіки хворіють в 4-5 разів частіше за жінок. Захворюваність на рак кукси резецированного шлунка в останні роки зростає. Пухлина частіше виникає через 10-20 років після операції. Ризик підвищується у людей, яким резекція шлунка виконана в молодому віці. Те, що раніше називалося терміном «пізні рецидиви раку оперованого шлунка», за деякими даними, є новою пухлина, яка виникла внаслідок рефлюксу жовчі в куксу шлунка.
Хворі, які перенесли резекцію шлунка 10 років і більше тому, повинні щорічно проходити огляд лікаря з обов'язковим ендоскопічним або рентгенологічним обстеженням.
Класифікація. Залежно від локалізації виділяють рак кардіального відділу, рак тіла (мала і велика кривизни, передня і задня стінки) і рак антрального відділу шлунка. Найчастіше пухлина вражає антральний відділ шлунка (60% спостережень). На малій кривизні карцинома розвивається у 20-25% хворих, на передній і задній стінках - в 2-5% спостережень, в проксимальних відділах - у 10-15% пацієнтів, тотальне ураження реєструють у 5% пацієнтів, а велика кривизна шлунка уражається у 1-3% хворих.
Макроскопічно розрізняють три типи росту раку шлунка (екзофітний, ендофітний і змішаний). З ними можна зв'язати особливості клінічної симптоматики захворювання та характер метастазування.
Екзофітний зростання пухлини характеризується чіткими її межами. При екзофітної раку новоутворення має вигляд поліпа, бляшки або гриба.
При виразці такої пухлини її цін тр набирає вигляду блюдця. На відстані більше 2-3 см від видимого краю пухлини ракова інфільтрація зазвичай не поширюється.
Найбільш злоякісно протікає рак шлунка, що відрізняється ендофітний (інфільтративний) типом росту. Ці пухлини не вдаються в просвіт органа і не мають чітких меж. Інфільтративні карциноми поширюються уздовж стінки шлунка, головним чином по підслизовому шару, багатому лімфатичними судинами, і частіше метастазують. Складки слизової оболонки шлунка при цьому розправляються, згладжуються. При мікроскопічному дослідженні видаленого препарату клітини раку можна виявити на відстані 5-7 см від макроскопічно передбачуваної кордону пухлини.
При змішаному типі поєднуються ознаки екзо і ендофітний зростання. У цих випадках перебіг захворювання визначає інфільтративний компонент пухлини.
Міжнародна гістологічна класифікація поділяє рак шлунка наступним чином.
за ступеня диференціювання пухлинних клітин міжнародна класифікація передбачає високо-, помірно і низькодиференційовані види аденокарцином. Слід зазначити, що в межах однієї пухлини можуть виявлятися ділянки різної будови і різного ступеня диференціювання. Це пояснюється складністю будови слизової оболонки шлунка, здатністю її камбіальних клітин диференціюватися в морфологічно і функціонально різні клітинні елементи.
Міжнародна класифікація раку шлунка (TNM, див. примітку на с. 71):
- Т - первинна пухлина:
ТХ - недостатньо даних для оцінки первинної пухлини;
ТО - первинна пухлина не визначається;
Tis - преінвазивного карцинома: інтраепітеліальна пухлина без інвазії власної пластинки слизової оболонки (carcinomainsitu);
Т1 - пухлина інфільтрує слизову і підслизовий шар;
Т2 - пухлина проростає м'язовий шар, субсерозну оболонку;
ТЗ - пухлина проростає серозну оболонку (вісцеральну очеревину) без і н ваз і і в сусід н і е стру ктура и;
Т4 - пухлина поширюється на сусідні структури (селезінку, поперечну ободову кишку, печінку, діафрагму, підшлункову залозу, черевну стінку, наднирники, нирки, тонку кишку, заочеревинного простору);
- N - регіонарні лімфатичні вузли:
NX - недостатньо даних для оцінки регіонарних лімфатичних вузлів;
N0 - немає ознак метастатичного ураження регіонарних лімфатичних вузлів;
N1 - є метастази в 1-6 регіонарних лімфатичних вузлах;
N2 - є метастази в 7-15 регіонарних лімфатичних вузлах;
N3 - є метастази більш ніж в 15 регіонарних лімфатичних вузлах;
- М - віддалені метастази:
MX - недостатньо даних для визначення віддалених метастазів;
МО - немає ознак віддалених метастазів;
М1 - є віддалені метастази.
Групування за стадіями представлена в табл. 13.1.
Таблиця 13.1
Груніровка раку шлунка але стадіями
|
стадія |
характеристика no TNM (Див. Прим, на с. 71) |
||
|
первинна пухлина |
регіонарні лімфатичні вузли |
віддалені метастази |
|
|
0 |
Tis |
N0 |
МО |
|
I а |
T1 |
N0 |
МО |
|
lb |
T1 |
N1 |
МО |
|
T2 |
N0 |
МО |
|
|
II |
T1 |
N2 |
МО |
|
T2 |
N0 |
МО |
|
|
тз |
N0 |
МО |
|
|
III |
T1 |
N.2 |
МО |
|
Т2 |
N1 |
МО |
|
|
ТЗ |
N0 |
МО |
|
|
I Ua |
Т2 |
N2 |
МО |
|
тз |
N1 |
МО |
|
|
Т4 |
N0 |
МО |
|
|
III b |
ТЗ |
N2 |
МО |
|
IV |
Т4 |
N1 - N3 |
МО |
|
Т1 - ТЗ |
N.3 |
МО |
|
|
Будь-яка Т |
Будь-яка N |
М1 |
|
Рак шлунку метастазує переважно лімфогенним шляхом. Можливі також гематогенний, контактний або імплантаційний шляху поширення пухлини. Найчастіше відзначається наступна послідовність метастазування: спочатку уражаються регіонарні лімфатичні бар'єри (лімфатичні вузли, розташовані в зв'язках шлунка), потім лімфатичні вузли, які супроводжують великі артерії, що живлять шлунок, потім зачеревні лімфатичні вузли і органи черевної порожнини.
В даний час детально описані 20 груп регіонарних лімфатичних вузлів, які формують три послідовні (не в істинному розумінні послідовності) етапу метастазування від різних відділів шлунка - від N1 до N3.
Залучення лімфатичних колекторів N1 - N2 розглядають як регионарное метастазування, тоді як залучення лімфатичних вузлів N3 - як віддалене метастазування.
Карцинома шлунка має схильність більшою мірою поширюватися вгору по шлункової стінки відповідно переважного току лімфи в сторону малої кривизни шлунка і шлунково-підшлункової зв'язки, де розташований головний колектор лимфооттока від шлунка.
Гематогенно найбільш часто рак шлунка метастазує в печінку. Рідше метастази виявляють у легенях, підшлунковій залозі, надниркових залозах, кістках.
Для раку шлунка характерними віддаленими метастазами вважаються:
Клінічна картина і діагностика. Ранній рак шлунка клінічних проявів, на жаль, не має. Всі скарги хворих пов'язані з іншими тривало існуючими хронічними захворюваннями шлунка. Симптоми раку шлунка на початку захворювання характеризуються переважно тими функціональними порушеннями, які є в доопухолевой фазі розвитку або типові для передракових захворювань. Основні труднощі ранньої діагностики раку шлунка полягають в прихованому перебігу даного захворювання в доклінічній стадії, а скарги пацієнтів нічим не відрізняються від таких при доброякісних ураженнях шлунка запального або функціонального характеру. Причому латентний перебіг буває досить тривалим, а симптоми з'являються у міру зростання пухлини.
Залежно від фону, на якому розвивається пухлина, прийнято розрізняти три клінічних типу захворювання:
Клінічна класифікація, запропонована С. А. Холдинг, вказує на частоту окремих форм раку як в ранній, так і в більш пізніх фазах. Відповідно до цієї класифікації виділяють чотири типи раку шлунка:
Ці найбільш вдалі клінічні класифікації підкреслюють ряд моментів, які слід пам'ятати:
Першими проявами раку шлунка найчастіше бувають невмотивовані і нерідко невизначені диспепсичні скарги, в інших випадках провідним симптомом може бути прогресуюча анемія, наростаюча слабкість і схуднення. У ряді випадків захворювання проявляється шлунково-кишковою кровотечею. Є синдром «малих ознак» (в лапках, тому що найчастіше це ознаки великої пухлини, часом неудалімой). Якщо лікар у поліклініці, вперше досліджує хворого похилого віку, яка поставила ряд шлункових скарг, буде «онкологічно насторожений», то він зуміє звернути увагу і надати значення самих незначних проявів захворювання, як то: невизначений відчуття важкості після їжі (дискомфорт), відрижка, іноді незначні болі. Цього вже достатньо, щоб направити пацієнта в онкологічний кабінет.
У синдром «малих ознак» входять такі симптоми, як стомлюваність, втома, неадекватні виконуваній роботі; зниження апетиту, відчуття важкості після їжі, прогресуюче схуднення, незначна анемія, апатія і ряд інших. Кожен з цих симптомів непатогномоні- чен для раку шлунка, він зустрічається і при інших захворюваннях, наприклад при хронічному гастриті. Комбінація цих ознак дозволяє запідозрити рак шлунка, особливо якщо мова йде про літнього хворого, і направити його на ендоскопічне дослідження з можливою біопсією, яке виявляється вирішальним у постановці діагнозу. Однак, як показав подальший багаторічний досвід, синдром «малих ознак» більше характерний для вже досить поширених форм раку шлунка.
Наростання симптоматики відбувається у міру зростання пухлини і порушення внаслідок цього функції та структури органу. При поширенні пухлини на зону кардії і стравохід приєднуються дисфагія і рясна салівація. У разі скарг хворого на почуття переповнення в епіга- Стрий, нудоту і блювоту з'їденої напередодні їжею є всі підстави запідозрити рак нижньої третини зі стенозом вихідного відділу шлунка.
При завзятій блювоті можуть розвинутися виражені водно-електролітні розлади аж до тетанії. Раку шлунка в більшості випадків можуть супроводжувати болі в епігастрії, в правому або лівому підребер'ї. Іррадіація болів в спину або поперек часто буває пов'язана з проростанням пухлини в підшлункову залозу або метастатичними враженнями заочеревинних лімфатичних вузлів.
Біль в животі - характерний симптом раку шлунка, проте він рідко буває початковим ознакою захворювання. Часто тільки через кілька місяців після появи шлункового дискомфорту приєднується біль. У хворих на рак шлунка зазвичай відзначаються ниючі, тупі, різної інтенсивності, частіше за все несильні, не пов'язані з прийомом їжі, не мають періодичності і сезонності болю в епігастральній ділянці. Різниця больового синдрому залежить:
Другим за значенням серед місцевих проявів вважається діспепті-
ний синдром, який знаходиться в прямій залежності від локалізації первинної пухлини. Найбільш часто диспептичний синдром спостерігається при пухлинах нижньої третини шлунка, коли внаслідок стенозу пілоруса порушується евакуація злиденні.
У міру зростання пухлини і прогресування стенозу вихідного відділу шлунка відрижка повітрям з неприємним запахом і їжею змінюється блювотою їжею, з'їденої напередодні.
Рак тіла шлунка тривалий час може протікати без виражених місцевих ознак. На перший план виступають розлади загального характеру. При виразці пухлин цієї локалізації може спостерігатися субфебрильна температура, а при пухлинах малої кривизни одним з перших проявів нерідко буває шлункова кровотеча.
дисфагія - симптом, найбільш характерний для раку, який локалізується в кардіальному відділі шлунка, але він не може вважатися раннім проявом захворювання.
Найбільш часто карцинома шлунка проявляється втратою маси тіла, особливо при раку, який супроводжується стенозом пілоруса. У деяких пацієнтів із злоякісними новоутвореннями шлунка внаслідок інтоксикації і розпаду пухлини буває гіпертермія.
Порівняно тривалий розвиток пухлини без місцевих симптомів відноситься до «німим» формам хвороби та зустрічається в 2-3% всіх випадків раку шлунка. Прихований рак шлунка іноді проявляє себе віддаленими метастазами без яких-небудь «шлункових» скарг. З появою ендоскопічної техніки ранні і «німі» форми раку шлунка стали виявляти при профілактичних дослідженнях. Як уже згадувалося, кожного хворого при наявності раку шлунка слід обстежити на предмет виявлення віддалених метастазів: Вірхова, Крукенберга, Шніцлера, сестри Джозеф. При наявності віддалених метастазів в печінку пальпаторно вона може бути щільною, збільшеною і горбистої. При огляді живота також необхідно звертати увагу на наявність або відсутність асцитичної рідини.
В цілому поліморфізм клінічних проявів раку шлунка залежить від багатьох причин, головні з яких - форма і локалізація пухлини в шлунку, будова і швидкість розвитку новоутворення, стадія процесу, розвиток ускладнень, темпи метастазування.
Клінічна діагностика раку шлунка починається з загального огляду пацієнта. Нерідко при поширених формах захворювання звертають на себе увагу блідість і землистий шкірних покривів, схуднення і зниження тургору шкіри. Слід зазначити, що при раку шлунка у 20-25% хворих розвивається залізодефіцитна анемія. Причинами анемії (поряд з можливою хронічної крововтратою) служить гемолізує вплив продуктів розпаду пухлини, пригнічення гемопоезу внаслідок атрофії слизової оболонки шлунка, відсутність соляної кислоти і втрата шлунком здатності виробляти антианемичний фактор Касла. Ретельне вивчення анамнезу захворювання дозволяє якщо не встановити, то, по крайней мере, запідозрити рак шлунка. Виявлення в анамнезі виразкової хвороби, поліпозу шлунка, хронічного гастриту з вираженою секреторною недостатністю та анемією (по типу пернициозной) повинні привернути увагу лікаря так само, як і зміни характеру хворого (поява плаксивості, дратівливості, неуважності і т. Д.).
пальпаторне виявлення освіти в епігастральній ділянці служить важливим місцевим ознакою пухлини шлунка. У 80-87% хворих в таких випадках вдається зробити радикальну операцію, проте, як правило, мова при цьому йде про пухлини, які локалізуються в нижній третині шлунка і зміщуються при пальпації. Якщо ж пухлина локалізується в лівому підребер'ї і нерухома, то резектабельность при раку шлунка сумнівна.
При великих пухлинах шлунка може визначатися притуплення перкуторного тону в епігастральній ділянці. У таких пацієнтів виконання радикальної операції вельми сумнівно.
Іноді при проростанні раку шлунка в великі артеріальні судини при аускультації у верхніх відділах живота вислуховуються систолічний шуми. Це свідчить про місцеве поширення ракового процесу, і, як правило, такі пухлини нерезектабельних.
Серед різноманітних атипових клінічних форм раку шлунка в даний час виділяють:
Основні ускладнення раку шлунка: кровотеча, перфорація, інфікування і проростання пухлини в сусідні тканини і органи.
Розглянемо особливості лабораторної діагностики. Клінічне дослідження крові в ранньому періоді хвороби рідко виявляє будь-які зміни. Анемія, як правило, розвивається вдруге внаслідок постійної крововтрати, недостатньою засвоюваності харчових речовин, зокрема заліза; при ахлоргідрії, а також при інтоксикації (при цьому може мати місце і лейкоцитоз). Зміна складу периферичної крові найбільш виражено при метастатичному ураженні декількох органів і буває при метастазуванні в печінку і підшлункову залозу, але менш виражено при заочеревинному проростанні пухлини.
При біохімічному дослідженні крові можуть бути виявлені діспро- теінеміі з тенденцією до гіпопротеїнемії, але частіше ці зміни відзначаються при запущених стадіях захворювання. Підвищення рівня лужної фосфатази і збільшення амінотрансфераза (АлАТ) і аспартатаміно- трансфераза (АСТ) в ряді випадків може вказувати па наявність віддалених метастазів в печінку, рідше - в кістки.
Незначні, приховані кровотечі супроводжують більшість випадків раку шлунка. Найбільш поширена проба для виявлення «прихованої» крові в калі - проба Грегерсена.
В останні роки для уточнення поширеності пухлинного процесу, особливо при III-IV стадіях захворювання, використовують визначення концентрації пухлинних маркерів (РЕА, СА 19-9, СА 72-4), а також білків гострої фази (орозомукоида, гаптоглобіну). Підвищення їх рівня свідчить про збільшення «сумарною маси пухлинних клітин», характерному для генералізованих форм захворювання, що в прогностичному плані несприятливо.
ендоскопічна діагностика набула широкого поширення в зв'язку з розробкою і впровадженням в клінічну практику ендоскопів на основі волоконної оптики (а тепер і цифрової апаратури), які дають можливість огляду всіх відділів шлунка і отримання матеріалу для морфологічного (гістологічного, цитологічного) дослідження. Із сучасних методів ендоскопії слід зазначити «зум-ендоскопію», яка дозволяє багаторазово (в сотні разів) збільшувати зображення структури пухлини при гастроскопії.
при рентгенологічному дослідженні застосовують контрастування барієвої суспензією - рентгеноскопію шлунка. Найбільш важливі рентгенологічні ознаки раку шлунка - це виявлення:
Рентгенодіагностика раннього раку шлунка практично неможлива.
фиброгастродуоденоскопия (ФГДС) з прицільною біопсією має перевагу перед рентгенологічним дослідженням у виявленні новерхностних, дуже маленьких пухлин. У той же час ендоскопічний метод поступається рентгенологічного дослідження у виявленні підслизової інфільтрації стінки шлунка, у визначенні причин і характеру деформації органу, часто обумовлених злоякісним процесом та ураженням стінки шлунка, причому коли слизова оболонка може бути незміненою.
Ультразвукове дослідження (УЗД) при раку шлунка проводиться трьома способами:
ендоскопічна ультрасонографія істотно розширює можливості діагностики раку верхніх відділів шлунково-кишкового тракту (див. параграф 13.3).
Незважаючи на значно більш високу роздільну здатність комп'ютерної томографії (КТ) та магнітно-резонансної томографії (МРТ), виразних переваг для визначення інтраорганних поширення пухлини вони не мають. Додаткова інформація може бути отримана для виявлення проростання пухлини в навколишні органи при зміні їх форми і взаємного розташування. У поєднанні з ангіографією вони дозволяють судити про проростання пухлини в великі кровоносні судини. Таким чином, основними MPT-симптомами раку шлунка є:
КТ і МРТ високоефективні для виявлення вогнищевих уражень паренхіматозних органів, збільшених лімфатичних вузлів у зонах регіонарногометастазування, а також для оцінки стану лімфатичних колекторів, які перебувають в середостінні, які недоступні для дослідження більш простими методиками.
Позитронно-емісійна томографія (ПЕТ) - новий метод діагностики злоякісних пухлин з використанням різних природних метаболітів, мічених радіоактивними ізотопами. В основі позитронно-емісійної сканування з фтордезоксіглюкози лежить відмінність в метаболізмі глюкози між нормальними і злоякісними клітинами. 18-фтор-2-дезоксиглюкоза накопичується клітинами пухлини в зв'язку з тим, що злоякісні клітини не можуть метаболизировать її в результаті фосфорилювання. На відміну від методів структурного сканування (УЗД, КТ, МРТ), ПЕТ - це варіант функціонального сканування з високою роздільною здатністю, що володіє специфічністю до 95%. Слід підкреслити, що ПЕТ застосовується не тільки для доопераційного визначення стадії пухлини, а й для оцінки результату операції і визначення ефективності проведеної хіміо- та радіотерапії.
лапароскопічну діагностику проводять з метою уточнення глибини поразки пухлиною стінки шлунка, зокрема виходу на серозну оболонку, виявлення поширення її на сусідні органи, виявлення метастазів в печінці, асциту і канцероматоза очеревини. Зіставлення лапароскопічних даних про проростання серозного покриву шлунка з даними морфологічного дослідження резецированного шлунка показало достовірність методу в 95% випадків. Лапароскопію слід виконувати всім пацієнтам раком шлунка, за винятком випадків раннього раку і ускладненого перебігу захворювання (стенози кардії або вихідного відділу шлунка, кровотеча), коли оперативне втручання роблять за життєвими показаннями незалежно від лапароскопічних знахідок.
Диференціальна діагностика. Захворювання, з якими необхідно диференціювати рак шлунка, можна розділити на дві групи: 1) захворювання шлунка і 2) захворювання, не пов'язані зі шлунком. До першої відносять виразкову хворобу, різноманітні форми гастриту, перигастрит, доброякісні новоутворення (поліпи, ліпоми, міоми, фіброми і т. Д.), Туберкульоз, сифіліс, актиномікоз, амілоїдоз, безоара і ін., До другої - пухлини і кісти печінки, підшлункової залози, внебрюшінние пухлини і новоутворення поперечної ободової кишки. При кардіоезо- фагеальном раку, що супроводжується дисфагією, слід проводити диференційну діагностику із захворюваннями стравоходу, в першу чергу, з ахалазії.
Лікування раку шлунка. В даний час, незважаючи на деякі успіхи комбінованих методів лікування, лише хірургічний метод залишається «золотим стандартом» при радикальному лікуванні раку шлунка. Тільки операція і видалення пухлини дозволяють сподіватися на повне одужання пацієнта.
Перші резекції шлунка з приводу раку були виконані майже одночасно різними хірургами: Ж. пеанів у Франції в 1879 р, Л. Рідігером в Польщі в 1880 р Ці операції мали летальні випадки. Лише 29 січня 1881 р професор віденського університету Т. Більрот вперше справив успішну резекцію шлунка з приводу раку. У Росії перша резекція шлунка була виконана в Санкт-Петербурзі М. К. Китаївська 16 червня 1881 року (через 5,5 місяці після Т. Більрот), але зі смертельним результатом. Першу успішну резекцію шлунка з приводу раку в Росії виконав в 1882 р Н. В. Екк. У 1884 р Ф. Коннор з Цинциннаті (США) вперше виконав гастректомію з приводу раку шлунка (з летальним результатом), а в 1897 р К. Шлаттер в Цюріху вперше з успіхом здійснив цю операцію (теж з приводу раку шлунка), ніж поклав початок хірургічного лікування раку тіла і проксимального відділу шлунка. Першу гастректомію в Росії справив відомий петербурзький хірург, професор С. П. Федоров в 1902 г. (але з летальним результатом), успішно ця операція вперше в Росії була виконана в 1911 р В. М. Зиковим в Москві.
радикальні операції з приводу раку завжди включали обов'язкове моноблочне видалення регіонарних лімфатичних вузлів. Вперше такий підхід був запропонований більш 100 років тому У. Холстедом при хірургічному лікуванні раку молочної залози. З тих пір це положення визначає стратегію онкохірургії в цілому і тактику оперативного лікування раку шлунка зокрема.
Поняття превентивної розширеної лімфодіссекціі було вперше введено при хірургічному лікуванні раку шлунка для позначення втручань, що супроводжуються плановим видаленням ураженого органу і зон регіонарного метастазування. Слід підкреслити, що термін «лімфодіссекція», будучи більш ємним, ніж термін «лімфаденектомія», включає моноблочне видалення не тільки лімфатичних вузлів, але і всього лімфатичного апарату (лімфатичних судин з оточуючою жировою клітковиною) в межах фасциальнихфутлярів.
В даний час використовують класифікацію лімфаденектоміі (лімфодіссекціі), засновану на категорії D (dissection):
DO - резекція з неповним видаленням вузлів групи N1 (Це пери гастральние лімфоколлекторов, розташовані в зв'язках шлунка, № 1-6);
D1 - резекція з повним видаленням вузлів групи N1 (Повне видалення вищевказаних лімфатичних вузлів, № 1-6);
D2 - резекція з повним видаленням вузлів групи N1 і N2 (До періга- стральним лімфоколлекторов зв'язкового апарату шлунка додають зачеревні лімфатичні вузли, розташовані по ходу гілок чревного стовбура: по ходу лівої шлункової артерії, загальної печінкової артерії, черевного стовбура, в воротах селезінки, по ходу селезінкової артерії);
D3 - резекція з повним видаленням вузлів групи N1, N2 і N3 (До вищевикладеним лімфатичних вузлів слід додати лімфовузли гепато- дуоденальної зв'язки, ретропанкреатодуоденальние, лімфатичні вузли по ходу верхньої брижової артерії, в корені брижі поперечної ободової кишки по ходу середньої ободової артерії, парааортальні лімфатичні вузли, розташовані на різних рівнях черевної аорти).
Слід підкреслити, що на сьогоднішній день лімфодіссекція D2 вважається стандартною.
В даний час в усьому світі при раку шлунка застосовують три основних типи радикальних операцій: гастректомія, субтотальна проксимальна резекція шлунка, субтотальна дистальна резекція шлунка.
гастректомія - повне видалення шлунка і всіх зон регіонарного метастазування з гістологічним дослідженням лінії проксимального і дистального перетину стінки стравоходу і ДПК (рис. 13.1). Її виконують при раку тіла шлунка будь макроскопічної форми зростання, местнораспространенной пухлини, а також у випадках субтотального або тотального ураження шлунка. Обов'язкова умова даної операції - наявність в віддаленому препараті слизової оболонки стравоходу і ДПК.
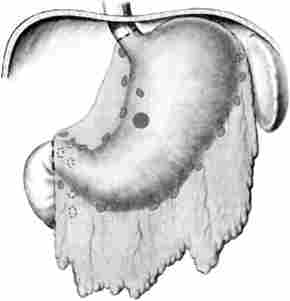
Мал. 13.1. Обсяг операції при резекції шлунка
При поширенні пухлини на розетку кардії, абдомінальний або діафрагмальний сегмент стравоходу слід одномоментно виконувати резекцію стравоходу з комбінованого лівостороннього торакоабдомінальної доступу.
Субтотальную проксимальную резекцію шлунка (рис. 13.2) чрезбрю- шинним доступом виконують тільки при екзофітної пухлини верхньої третини шлунка, що не розповсюджується на розетку кардії.
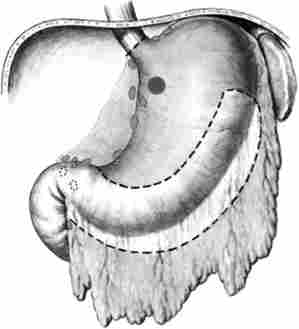
Мал. 13.2. Субтотальна проксимальна резекція шлунка. обсяг операції
Субтотальная дистальная резекція шлунка (Рис. 13.3) виконується в модифікаціях Більрот-I (формування прямого гастродуоденальної анастомозу) або Більрот-П (створення гастроеюнального соустя з одностороннім вимиканням ДПК).
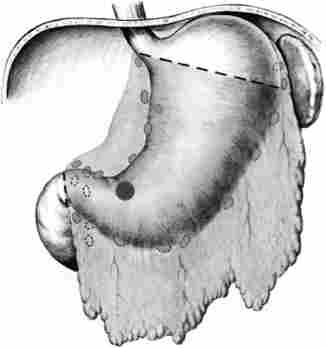
Мал. 13.3. Субтотальная дистальная резекція шлунка. обсяг операції
Більшість хірургів віддають перевагу операції по Більрот-П, а деякі з них - переконані противники резекції шлунка за першим способом Більрот при раку, вважають це втручання неадекватним з онкологічною точки зору. Разом з тим є дані, що за методикою Більрот-I можна виконати субтотальную дистальную резекцію шлунка з необхідною широтою видалення всього лімфатичного апарату з дотриманням принципів онкологічного радикалізму. Деякі хірурги виконують навіть гастректомію з накладенням прямого езофа годуоденоанастом оза.
Правильно вироблена з онкологічних міркувань мобілізація шлунка сприяє більшій рухливості його кукси, що збільшує шанси формування гастродуоденальної анастомозу без натягу. Слід зазначити, що операція по Більрот-I все ж більш фізіологічна, так як при цьому в якійсь мірі зберігається регуляція жовчовиділення при природному проходженні їжі по ДПК (при відсутності дуодено- сгаза (а це буває складно з'ясувати до операції), який призводить до розвитку дуодено-гастрального рефлюксу, що стає основним недоліком резекції шлунка по Більрот-I). Але основна перевага цієї операції полягає в тому, що не відбувається прямого контакту шлункової кукси зі слизовою оболонкою тонкої кишки, а це виключає найнеприємніше ускладнення дистальних резекцій - виразку соустя.
Використання гастродуоденальної анастомозу при раку шлунка (якщо це онкологічно виправдано, що не завжди можливо при виконанні субтотальної резекції шлунка) слід вважати кращим, тому що збереження пасажу їжі але ДПК дозволяє значною мірою поліпшити функціональні результати і якість життя пацієнтів, забезпечуючи в той же час необхідну онкологічну радикальність операції і хороший безпосередній результат.
На рис. 13.4 і 13.5 представлені різні модифікації резекцій шлунка але методикам Більрот-I і Більрот-П.
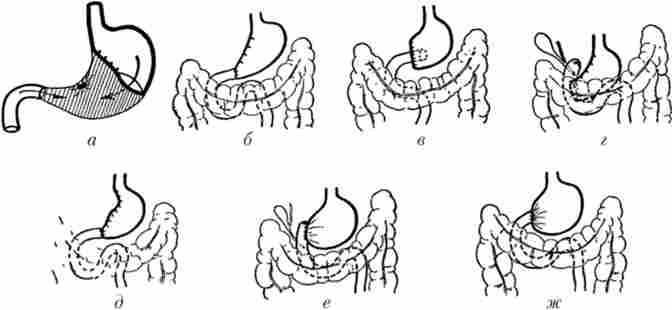
Мал. 13.4. Варіанти операції за методикою Більрот-1:
а - резекція за методом Більрот-I; б - спосіб Більрот; в - спосіб Кохера; г - спосіб Ейзельсберга; д - спосіб Шумейкер - Шмід; в - перший спосіб Хаберера; ж - другий спосіб Хаберера
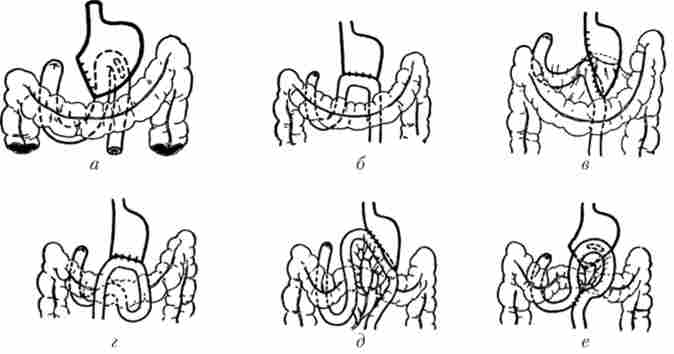
Мал. 13.5. Варіанти операції за методикою Більрог-Н:
а - спосіб Більрот; б - спосіб Сповнена - Рейхеля; в - спосіб Гофмейстера - Фінстерера; г - спосіб Мойніхана; д - спосіб Мейнгога; е - спосіб Бальфура
На рис. 13.6 представлені різні способи формування стравохідно-кишкових анастомозів при резекції шлунка.
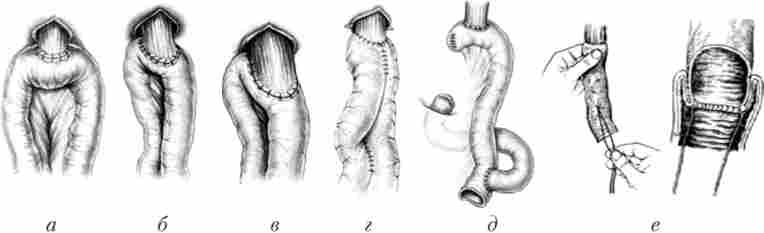
Мал. 13.6. Основні види езофагоеюноанастомоза:
а - горизонтальний езофагоеюноанастомоз кінець в бік (сполучення між стравоходом і горизонтальною частиною тонкої кишки); 6 - анастомоз але Макніру і Пеку; в - вертикальний езофагоеюноанастомоз кінець в бік з фіксацією до кишці розташованого вздовж неї стравоходу спеціальними швами (по Сапожкова - Юдина); г - анастомоз по Гілярович; д - анастомоз по Орру - Ханту - Накаяма; е - інвагінаціоіпий анастомоз по Цацаніді
Загальновизнане правило при раку - видалення пухлини в межах здорових тканин в єдиному блоці з усім зв'язковим апаратом шлунка, що включає регіональні лімфатичні вузли, найчастіше і в першу чергу вражаються метастазами карциноми.
Виникає питання: на скільки сантиметрів від країв пухлини повинна відстояти лінія резекції, щоб у хірурга була впевненість в радикальності втручання? За даними більшості авторів, при інфільтративно-виразкових формах раку шлунок слід перетинати, відступивши від краю пухлини не менше ніж на 8-10 см, а при обмежених, екзофітно зростаючих формах раку - не менше ніж на 6-8 см. В той же час роботами ряду дослідників встановлено, що при раку пілоричного відділу шлунка (в першу чергу - при ендофітний формах) можливе поширення пухлинних клітин по лімфатичних судинах підслизового і м'язового шарів на початкову частину ДПК. У зв'язку з цим необхідно видалення не менше 2-3 см кишки.
Субтоталиюй резекцією шлунка вважається та операція, при якій видаляють всю малу кривизну шлунка від стравоходу, а по великій кривизні шлунок перетинають на рівні нижнього полюса селезінки. При субтотальної дистальної резекції шлунка повністю січуть печінково шлункову зв'язку і перетинають ліву шлункову артерію у місця її відходження від чревного (біля основи) в товщі шлунково-підшлункової зв'язки, а також видаляють разом зі шлунком весь великий сальник (місце найбільш частою локалізації регіонарних метастазів) .
Показанням до субтоталиюй дистальної резекції шлунка служить екзофітний рак нижньої третини шлунка. За суворими показаннями виконання цієї операції допускається при невеликих ендофітний або змішаній формі зростання пухлин нілороантрального відділу, або коли маленька екзофітна пухлиналокалізується в середньої третини шлунка. Операцію завершують формуванням гастродуоденальної або гастроеюнального анастомозу. Найчастіше застосовують методику Більрот-II на довгій петлі худої кишки (по Бальфур) з ентеро-ентероанастомозом по Брауну між приводить і відводить петлями з метою профілактики рефлюкс-гастриту або на короткій петлі (але Гофмейстера - Фінстереру). Деякі хірурги віддають перевагу гастроеюнального анастомозу на виключеною по Ру петлі тонкої кишки.
В даний час триває пошук нових хірургічних підходів, що дозволяють сподіватися на поліпшення віддалених результатів лікування. Одним із шляхів вирішення даної проблеми є підвищення онкологічного радикалізму і резектабельності за рахунок виконання комбінованих (при проростанні пухлини в сусідні органи) і розширених оперативних втручань.
Протипоказанням до радикального хірургічного лікування раку шлунка виявляється IV стадія захворювання, що супроводжується асцитом (канцероматоз очеревини), жовтяницею на тлі множинних метастазів в обох частках печінки (генералізація пухлинного процесу).
паліативні втручання при раку шлунка мають велике значення: вони спрямовані на ліквідацію ряду ускладнень, значно обтяжують стан пацієнтів. Ці операції істотно не продовжують життя хворих, але тимчасово покращують якість життя і загальний стан. При раку шлунка виконують три основні типи паліативних втручань: паліативну резекцію, формування обхідних анастомозів і поживних свищів (гастростому).
Паліативну резекцію шлунка виробляють при невеликих «рухомих» пухлинах (частіше ускладнених кровотечею), в основному вихідного відділу шлунка за тією ж методикою, що і радикальну, але при наявності віддалених метастазів (IV стадія захворювання).
Обхідний гастроентероанастомоз - найбільш важлива операція, так як він ліквідує затримку вмісту шлунка: припиняється блювота, зникають скарги на тяжкість в енігастріі, значно полегшується самопочуття і хворий вірить в одужання. При раку нижньої третини шлунка обхідний гастроентероанастомоз - нескладне втручання, що дає хороші результати. Ряд хірургів рекомендують заднє сполучення, інші - переднє. Немає сумніву, що основною операцією слід вважати передній анастомоз на довгій петлі з міжкишкових анастомозу за Брауном.
гастростомія (Свищ для харчування хворого) при раку кардії стає основним паліативним втручанням.
застосування променевої терапії як самостійного методу лікування раку шлунка є малоефективним. Найчастіше використовують комбінований метод лікування - променеву терапію в поєднанні з хірургічним втручанням. Зазвичай застосовують передопераційне опромінення при раку проксимальних відділів шлунка.
хіміотерапію проводять при первинно-нерезектабельних раку шлунка, рецидивах і метастазах пухлини, а також після виконання паліативних оперативних втручань, пробних лапаротомий. Найчастіше для лікування застосовують 5-фторурацил (5-ФУ) і фторафур (інгібітори ферментів з групи піримідину) як у вигляді монотерапії, так і в складі різних схем поліхіміотерапії.
активну імунотерапію проводять в поєднанні з хірургічним лікуванням раку шлунка. Але ефективність і цього методу невелика.
Профілактика. Профілактика раку шлунка базується на своєчасному виявленні та адекватному лікуванні передракових захворювань і раннього раку шлунка. Основним завданням в цьому питанні є активне виявлення хворих з даною патологією. Виникає необхідність виділення груп ризику, що включають пацієнтів з прикордонними змінами слизової оболонки шлунка. Слід зазначити, що крім активної вторинної профілактики раку шлунка і методів масового скринінгу населення першорядне значення як і раніше має правильне обстеження пацієнтів з патологією шлунково-кишкового тракту, що звертаються до лікаря поліклініки.
Прогноз захворювання. Прогноз і віддалені результати хірургічного лікування раку шлунка залежать від стадії пухлинного процесу, макроскопічної форми і гістологічної структури карциноми, локалізації пухлини. П'ятирічна виживаність залежить від стадії захворювання і залишає при стадії I а - 95%, lb - 85, II - 54, III а - 37,1 lib - 11, IV - менш 7%.
Комбіноване лікування операбельного раку шлунка збільшує тривалість безрецидивної життя хворих.