| Головна |
| «« | ЗМІСТ |
|---|
Лікування перитоніту має починатися з передопераційної підготовки. Обсяг і терміни її проведення залежать від характеру перитоніту, вираженості порушень гомеостазу та гемодинаміки. В середньому вона не повинна перевищувати 2 ч, так як без хірургічної корекції розраховувати на помітне поліпшення стану хворого не доводиться.
Особливо актуальними є питання передопераційної підготовки при поширеному перитоніті в термінальній стадії. Клінічний досвід показує, що втручання без відповідної підготовки, як правило, закінчуються летальним результатом.
Підготовка пацієнта до операції починається відразу ж після встановлення діагнозу аж до транспортування в операційну з послідовним переходом до багатокомпонентної загальної анестезії з використанням штучної вентиляції легенів. Схема передопераційної підготовки, як правило, стандартна і включає в себе: знеболювання; інфузійну терапію кристалоїдними і колоїдними розчинами; антибактеріальні препарати; профілактику тромбоемболічних ускладнень; катетеризацию сечового міхура; дренування шлунка; підготовку операційного поля. При наявності супутньої патології проводиться її корекція.
Принципова послідовність хірургічних маніпуляцій при поширеному перитоніті - це лапаротомія, видалення патологічного ексудату, ліквідація джерела перитоніту, санація черевної порожнини, дренування кишечника (за показаннями) і черевної порожнини. Також оперують хірургом приймається рішення про ушивання лана- ротомной рани або фомірованіі ланаростоми; доцільності проведення санаційних релапаротомії.
При поширеному перитоніті показано проведення серединної лапаротомії, яка забезпечує можливість адекватної ревізії і санації черевної порожнини. Використання доступів типу Мак-Берні (див. Гл. 22) можливо лише при місцевому характері перитоніту або після етапу діагностичної лапароскопії.
Після виконання доступу проводиться видалення патологічного вмісту, що сприяє повноцінній ревізії органів черевної порожнини. Крім цього, вміст черевної порожнини обов'язково направляється на мікробіологічне дослідження (посів на мікрофлору і визначення чутливості до антибіотиків), що дозволяє скорегувати антибактеріальну терапію в післяопераційному періоді.
На наступному етапі оператор усуває джерело перитоніту або відмежовує його від вільної черевної порожнини в разі неможливості одномоментного видалення або тяжкості стану пацієнта.
Після усунення джерела перитоніту важлива роль відводиться ретельної санації черевної порожнини з метою максимального видалення з неї мікрофлори, рідини і фібрину. Для цього використовується промивання порожнини різними розчинами антисептиків з наступною аспірацією рідини електричним відсмоктувачем. Успішний результат лікування хворого з найбільш важкою формою абдомінальної інфекції - перитоніт - на 80% визначається ефективністю хірургічної санації і лише на 15-20% залежить від ефективної антибактеріальної терапії.
Методика інтраопераційної санації залежить від причини, що викликала перитоніт. При невеликому терміні його розвитку в результаті перфорації виразок шлунка і дванадцятипалої кишки (до 12 год) обмежуються промиванням черевної порожнини двома-трьома літрами антисептика або ізотонічного розчину хлориду натрію. У більш пізні терміни, незалежно від причини, що викликала перитоніт, використовують більшу кількість розчинів (до восьми-десяти літрів) для санації, ретельно промиваючи черевну порожнину і поетапно видаляючи при цьому гній, фібрин, некротизовані тканини, шматочки харчових мас. У всіх хворих при санації черевної порожнини слід користуватися розчином, підігрітим до температури тіла.
Однак, навіть застосовуючи сучасні методи (різні антисептичні розчини, ультразвукову санацію), виконати повноцінне видалення інфекційного агента з черевної порожнини під час операції не завжди представляється можливим через що виникають технічні труднощі, викликаних деструктивним процесом і порушенням взаємин між органами. Найретельніший інтраопераційної лаваж не дозволяє промити всі відділи черевної порожнини, оскільки між складками очеревини залишається патогенна мікрофлора. Це диктує необхідність застосування методів виведення патогенної мікрофлори з черевної порожнини і в післяопераційному періоді, що досягається адекватним дренуванням. Крім цього, при вираженому парезі тонкої кишки необхідно провести назогастроінтестінальное дренування з метою декомпресії та видалення токсинів. Даний вид дренування здійснюється зондами типу зонда Еббота - Міллера.
При неможливості виконання цієї процедури (анатомічні особливості носових ходів, пілородуоденальний стеноз, виражений спайковий процес у верхніх відділах живота, небезпека розвитку дихальних розладів у літніх пацієнтів) можливе використання декомпресії кишечника через гастростому (рис. 24.2) або цекостому (рис. 24.3).
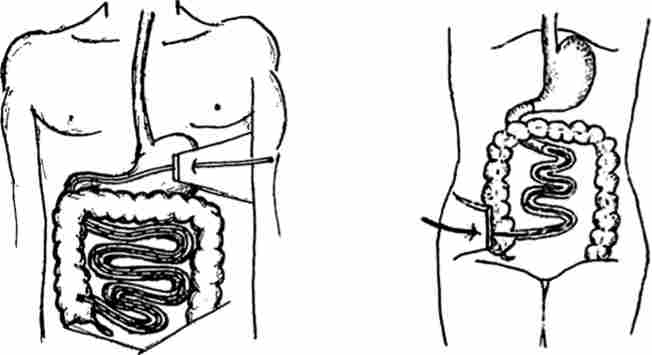
Мал. 24.2. Інтубація тонкої кишки через гастростому по Ю. М. Дедерер
Мал. 24.3. Інтубація тонкої кишки через цекостому по І. Д. Жітшоку
Показання до дренування черевної порожнини при перитоніті визначаються насамперед характером запалення очеревини (форма, поширеність, стадія процесу). У разі місцевого перитоніту рішення про дренуванні приймає оперує хірург на підставі інтраопераційних знахідок. Як правило, в таких ситуаціях буває досить одного дренажу, виведеного через контрапертуру.
При поширеному перитоніті черевну порожнину дренують в правому і лівому підребер'ї, розташовуючи дренажі йод печінкою і лівим куполом діафрагми, в обох клубових областях: справа - в бічному каналі, зліва - в порожнині тазу. Всі дренажі слід розташовувати уздовж стінок черевної порожнини, так як приміщення їх між петлями кишечника служить причиною ранньої та пізньої спайкової кишкової непрохідності (рис. 24.4).
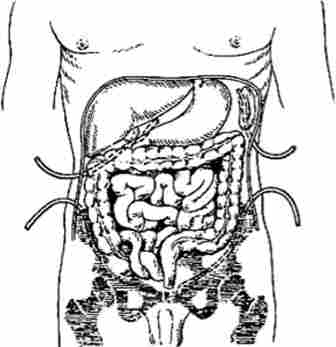
Мал. 24.4. Обов'язкові місця дренування черевної порожнини при розповсюдженому перитоніті
Для кожної форми перитоніту характерні свої особливості поширення інфекції по черевної порожнини. Тому область накладення контрапертури повинна бути визначена в залежності від патології, що викликала перитоніт. Дренування потрібно виконувати таким чином, щоб через додаткову рану не відбулася евентрація кишечника або іншого органу. Дренажні трубки при перитоніті нетривалий час здійснюють відтік ексудату, швидко відмежовуються, просвіт їх закривається, і вони перестають функціонувати. Використання рукавиць-марлевих дренажів і марлевих тампонів при перитоніті можливе лише з метою відмежування запального процесу (за умови неможливості його одномоментного видалення) від неураженоїобластей черевної порожнини.
Останнім часом набули розвитку лапароскопічні методики санації черевної порожнини при перитоніті, чому сприяли вдосконалення ендовідеохірургічним техніки і розробка оперативних прийомів.
Відеолапароскопічна санація складається з декількох етапів.
Перший етап - діагностичний. Він полягає у визначенні ступеня вираженості патологічного процесу в черевній порожнині. При цьому оцінюються характер і кількість перитонеального ексудату, запальні зміни очеревини, дилатація кишкових петель, стан перистальтики і швів анастомозів. За результатами діагностики визначаються показання до відсолапароскопі- чеський санації або до відкритого втручання.
Другий етап - проведення лікувальних процедур. З цією метою в живіт вводяться додаткові троакари з маніпуляторами в кількості від одного до трьох. Для санації нижнього поверху черевної порожнини їх розміщують в клубових і надлобковій областях, верхнього поверху - в епігастральній і мезогастральной областях.
Для адекватного огляду органів черевної порожнини доцільно використовувати кілька точок для установки оптичного троакара.
Санація черевної порожнини проводиться з використанням іррігаціонно- аспіраційної канюлі, що дозволяє як подавати рідину, так і видаляти її. При цьому доцільно міняти положення тіла хворого, надаючи операційного столу різні нахили: Фовлсра (піднятий головний кінець операційного столу), Тренд їв енбурга (піднятий ніжний кінець операційного столу), в бічні сторони. По можливості необхідно домагатися повного очищення вісцеральної і парієтальної очеревини від накладень фібрину, обережно розділяючи межпетлевих зрощення. Завершити лапароскопічну санацію слід дренированием черевної порожнини. Локалізація і число дренажних трубок залежать від поширеності перитоніту.
Наступний важливий етан в лікуванні перитоніту - післяопераційний період.
Обов'язковим компонентом лікувальних заходів виступає знеболення. Відразу після оперативного втручання призначаються анальгетики (наркотичні та ненаркотичні). Крім того, при стабілізації стану хворого можливе проведення пролонгованої епідуральної анестезії з анальгезуючою метою.
Велике значення в комплексному лікуванні перитоніту має антибактеріальна терапія. Використовується внутрішньом'язове, внутрішньовенне, Внутрішньоаортальної, внутрішньоартеріальне, ендолімфатичне введення антибіотиків. Як правило, на практиці перевага віддається внутрішньовенному шляху введення цих препаратів через периферичний або центральний венозний катетер. Місцеве застосування антибіотиків (при санації черевної порожнини або через залишені дренажі) в умовах системної антибактеріальної терапії недоцільно. Це пояснюється низькою ефективністю препаратів в умовах запаленої очеревини і високим ризиком місцевого токсичного ефекту.
Антибактеріальна терапія повинна відповідати ряду умов. Після операції вона призначається емпірично (в залежності від джерела перитоніту і можливих збудників) до отримання результатів мікробіологічних досліджень випоту з черевної порожнини. Схема антибактеріальної терапії повинна бути направлена на запобігання триваючого реінфікування в осередку інфекції. Антибіотики - основні препарати для лікування внебрюшних ускладнень перитоніту. Необхідно враховувати побічні ефекти лікування і супутню патологію. Найбільш поширені схеми емпіричної антибактеріальної терапії:
Іноді в процесі лікування виникає необхідність в зміні антибактеріальних препаратів. Пов'язано це або з отриманням результатів мікробіологічних досліджень (призначаються препарати, чутливі до даного виду інфекції), або при неефективності проведеної терапії (використовують антибіотики резерву - карбапенеми, цефалоспорини IV покоління).
У ранньому післяопераційному періоді є порушення водно-електролітного балансу, кислотно-лужного стану, які залежать від поширеності запального процесу в черевній порожнині і тяжкості стану хворого. Основним принципом інфузійно-дсзінтоксікаціонной терапії перитоніту вважається створення керованої гемодилюції. Обсяг рідини, що вводиться в період гострої інтоксикації досягає 4-5 л на добу. Додаткова терапія визначається ступенем вираженості водно-електролітних змін.
Як традиційної терапії застосовуються складні розчини (Рінгера, Хартмана), що містять в певних співвідношеннях всі необхідні електроліти. Обсяг інфузії цих розчинів становить від 1,5 до 3 л. Для ліквідації гіповолсміі застосовують колоїдні розчини (гслофузін, тстраспан) і білкові препарати крові (плазма, альбумін), поєднуючи їх з кристалоїдними розчинами. Обсяг необхідних середовищ для парентерального харчування визначають залежно від загального обсягу вводяться рідин, маси тіла і віку хворого. Виходячи з середньої добової потреби (до 3000 ккал), 2/3 його забезпечують за рахунок концентрованих розчинів глюкози, а 1/3 - за рахунок жирових емульсій (20% розчин Інтраліпіду, ліпофундін). Дедалі більшого поширення на практиці отримують сучасні препарати для парентерального харчування, такі як нутріфлекс, олікліномель, Кабівен. Вони являють собою збалансовану суміш, що складається з глюкози, електролітів, амінокислот і жирових емульсій.
Важливий метод детоксикації - форсований діурез. Цей метод найбільш простий за технікою виконання і не потребує спеціальної апаратури. Стимуляції функції нирок передує введення трансфузійних середовищ, які забезпечують помірну гемодилюцію. Попередню водне навантаження здійснюють за наступною схемою: вводять: 1000 мл розчину Рінгера - Локка, 500 мл 3% розчину бікарбонату натрію і 400 мл реоіоліглюкіна, після чого вводять діуретики - 40-80 мг лазиксу - і продовжують вливання 5% розчину глюкози (всього 1000- 1500 мл) і білкових препаратів (плазма крові, розчин альбуміну, білковий гідролізат). В цілому хворий отримує 4000-5000 мл рідини і виділяє 3000-4000 мл сечі. В ході виконання форсованого діурезу проводять погодинний облік кількості введеної рідини і виділеної сечі (по постійному катетеру 300-400 мл сечі за годину). Важлива умова адекватності проведеного форсованого діурезу - контроль за електролітним, білковим балансом організму, кислотно-лужним станом, змістом залишкового азоту, центральним венозним тиском.
В основі розвитку ендогенної інтоксикації лежить порушення функції детоксицирующих органів і систем (в першу чергу печінки і нирок). Тому в боротьбі з ендогенною інтоксикацією високоефективними виявилися методи, засновані на адсорбції токсичних речовин з крові і лімфи. Застосування їх виправдано при стабільній гемодинаміці пацієнта і гарантованої ліквідації джерела перитоніту.
гемосорбция дозволяє швидко знижувати критичні показники порушеного гомеостазу - підвищені рівні креатиніну, сечовини, білірубіну і т. д. Значно повільніше змінюється загальний токсичний фон крові - вміст «молекул середньої маси», некротичних тіл, що циркулюють імунних комплексів. У той же час при гемосорбції до третього-п'ятого дня лікування зменшується вміст еритроцитів, лейкоцитів, тромбоцитів периферичної крові в середньому на 10-40%, посилюється гипопротеинемия.
лімфосорбції дає можливість добитися стійкого детоксикаційної ефекту на рівні лімфи і крові, позитивно впливати на рівень основних класів імуноглобулінів, сприяє якісному поліпшенню дренажної функції лімфатичної системи і евакуації дегенеративно-запальних елементів із зони запалення і некрозу. Однак при лімфосорбції відбувається природна втрата формених елементів, наявних в лімфі. В результаті тривала лимфосорбция пригнічує імунні реакції організму, що вимагає проведення імунокорекції.
при плазмаферезе, що супроводжується видаленням до 2000 мл плазми хворого, не відзначається істотних втрат еритроцитів і тромбоцитів, а також клінічних ознак імунодефіциту. Проведення плазмаферезу на тлі анемії чи не поглиблює її, а сприяє підвищенню показників еритроцитів і гемоглобіну в результаті зниження токсичності крові хворого. Плазмаферез сприяє зменшенню вмісту «молекул середньої маси», некротичних тіл, що циркулюють імунних комплексів і зниження протеолітичної активності крові.
для застосування ультрафіолетового опромінення аутокрові з оксигенацией, гіпербаричної оксигенації при поширеному перитоніті практично не існує протипоказань. Ці методи детоксикації в поєднанні з традиційною інфузійної терапією дозволяють зменшити в'язкість крові, поліпшити її реологічні властивості. Їх призначення сприяє зменшенню концентрації «молекул середньої маси» і циркулюючих імунних комплексів.
Для профілактики ентеральної недостатності використовують такі лікувальні заходи:
Хороші результати в боротьбі з парезом кишечника отримані при тривалій епідуральної анестезії. Під її дією відбувається раннє відновлення перистальтики кишечника, відходження газів і відновлення самостійного стільця.
В якості профілактики тромбоемболічних ускладнень і для поліпшення мікроциркуляції крові застосовують низькомолекулярні генаріни (клексан, фраксііарін).
В даний час застосовуються два методи лікування поширеного перитоніту: «на вимогу» і «але програмі». У першому випадку проведення санаційних релапаротомії після завершення первинної операції не планується. У другому - під час первинної операції відразу ж планується етапна санація черевної порожнини. Терміни її проведення залежать від тяжкості стану пацієнта, стадії перитоніту, обсягу передбачуваного втручання і в середньому становлять 24 год після виконаної лапаротомії. Показаннями до застосування запрограмованих санацій черевної порожнини служать наступні інтраопераційні дані:
При виборі лікувальної тактики «на вимогу» релапаротомии здійснюються: при прогресуванні перитоніту, розвитку інтраабдомі- нальних ускладнень (в тому числі ятрогенних), виникненні конкуруючої хірургічної патології, розвитку синдрому интраабдоминальной гіпертензії. До внутрішньочеревним ускладнень перитоніту відносяться: абсцеси черевної порожнини, спайкова кишкова непрохідність, евен- трація, неспроможність швів порожнистих органів, формування кишкових свищів, післяопераційний кровотеча в черевну порожнину або в просвіт шлунково-кишкового тракту.
Для контролю за станом органів черевної порожнини велике значення має динаміка внутрішньочеревного тиску (ВБД). Вимірювання проводять непрямими методами: через сечовий міхур або шлунковий зонд. Интраабдоминальная гіпертензія (ІАГ) - це постійно або періодично (але нс короткочасно) реєстроване патологічне перевищення ВБД 12 мм рт. ст. Виділяють чотири ступені ІАГ:
I - ВБД 12-15 мм рт. ст .;
II - ВБД 16-20 мм рт. ст .;
III - ВБД 21-25 мм рт. ст .;
IV - ВБД> 25 мм рт. ст.
Синдром ІАГ - це стійке підвищення ВБД більше 20 мм рт. ст., яке супроводжується органної недостатністю або дисфункцією. В даний час хірургічна декомпресія - єдиний ефективний метод лікування синдрому ІАГ, без її проведення летальність досягає 100%.
У важких клінічних ситуаціях, таких як анаеробний перитоніт, синдром интраабдоминальной гіпертензії, а також при неможливості закриття рани передньої черевної стінки внаслідок се запальних змін вдаються до відкритого ведення черевної порожнини після оперативного втручання - лапаростоміі. Дана методика полягає в тампонування рани лапаротомного без її ушивання. Для профілактики можливої евентрації живіт пацієнта зав'язують простирадлом. В післяопераційному періоді щодня, під загальним знеболенням або продовженої епідуральної анестезією, проводять санацію черевної порожнини шляхом евакуації з неї гнійного ексудату, промивання антисептиками.
На сьогоднішній день одним з найбільш перспективних методів відкритого ведення черевної порожнини служить вакуум-терапія. Суть методу полягає в тому, що рана передньої черевної стінки герметизується з використанням клеїться плівки і через дренажну трубку створюється розрідження в черевній порожнині. Перевага методу - відсутність безлічі дренажів, а також можливість проводити етапні санації черевної порожнини не щодня, а раз на 2-3 доби. Невелика кількість спостережень поки не дозволяє рекомендувати методику до широкого впровадження в клінічну практику.
Показаннями до припинення етапних санацій і ушивання черевної стінки наглухо служать:
Основні ексграабдомінальние ускладнення перитоніту представлені органо-системної дисфункцією (недостатністю), нозокомиальной пневмонією - інфекцією нижніх дихальних шляхів, яка розвинулася у хворого після надходження в стаціонар; уроінфекціі; катетерной інфекцією. Для їх профілактики та лікування основне значення має адекватна антибактеріальна терапія.
Летальність при поширених формах перитоніту в токсичній і термінальній стадіях досягає 25-30%, а у випадках розвитку інфекційно-токсичного шоку і поліорганної недостатності - 74-80%.