| Головна |
| «« | ЗМІСТ | »» |
|---|
У реакціях другої фази ксенобіотики асоціюються з гідрофільними ендогенними сполуками. В результаті загальна гідрофільність збільшується настільки, наскільки необхідно для швидкого виведення речовини з організму. Як ендогенних гідрофільних речовин найчастіше виступають глюкуроновая кислота, метильние, ацетильную або сульфогрупи, глутатіон і гліцин. Ферменти, які беруть участь в цих реакціях, знайдені практично у всіх організмах: в бактеріях, дріжджах, рослинах і у всіх видах тваринного світу.
Значна кількість реакцій другої фази біотрансформації є реакції біоінактіваціі. Однак існує ряд винятків, в яких спостерігається протилежний ефект.
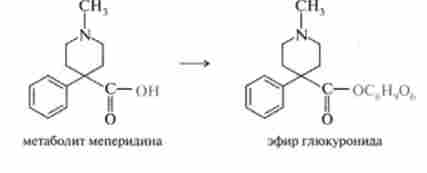
Серед реакцій кон'югації найбільш важливими в кількісному відношенні є реакції освіти глюкуронидов. Слід зазначити, що кон'югація субстрату з глюкуроновою кислотою може мати місце тільки після активації останньої. Освіта глюкуронидов є двохстадійною процесом, який включає, по-перше, біосинтез коферментной донора, УДФГК і, по-друге, перенесення за допомогою УДФ-трансглюкуронідаз глюкуронідного частини УДФГК на агликон:

Глюкуронідні кон'югати ксенобіотиків мають (5-піранозідной структурою і класифікуються наступним чином.
О-глюкуронід утворюються з фенолів, спиртів і карбонових кислот. наприклад:
N-глюкуронід відомо кілька типів. Атом азоту цих сполук, до якого приєднується глюкуронідного частина, може перебувати в аминогруппе, сульфамідної групі, карбомільной групі або в гетероциклічних азотистом з'єднанні.
S-глюкуроніду - тіоловою з'єднання з глюкуроновою кислотою, наприклад, глюкуроніди утворюються з тіофеноли, 2-меркаптобензтіозола і ін .:

Р-глюкуронідазу - фермент, гідролізу глюкуроновис кон'югати з вивільненням глюкуронової кислоти і агликонов. Цей фермент знаходиться в більшості тканин тваринного організму, наприклад в печінці, нирках, ендокринних залозах, селезінці. Деякі форми тканинної (3-глю- куронідази нс пов'язані з гідролізом чужорідних сполук, і, можливо, їх функція полягає в регуляції гормональної активності за допомогою вивільнення активних гормонів з неактивних глюкуронідних кон'югатів.
Іншим загальним класом кон'югатів є складні ефіри сірчаної кислоти або ефірсульфати. Існує кілька різних типів ефір- сульфатів, в тому числі:
арілсульфати - складні ефіри фенольних сполук, наприклад феніл сульфат;
алкілсульфати - складні ефіри первинних аліфатичних спиртів, наприклад етілсульфат;
сулирамати - складні ефіри сірчаної кислоти та амінів, що містять сульфамідної групу, наприклад фенілсульфамід;
стероїдні сульфати - складні ефіри первинних спиртових груп стероидной бічного ланцюга, наприклад ранолсульфат;
вуглеводні сульфати - складні ефіри гідроксильних ipynn вуглеводів, наприклад хондроітілсульфат.
Ферментативний гідроліз ефірсульфатов каталізується групою гідро- лаз - сульфатаз, з яких найбільше значення має арилсульфатазу.
Часто в якості кон'югується агентів ідентифікують метшьние групи. Метилирование - звичайна біохімічна реакція - полягає в перенесенні метильних груп від коферменту 5-аденозил метіоніну на аміни, феноли і тіоловою з'єднання з утворенням А-, О і 5-мстілових кон'югатів, причому мстільние групи переносяться на субстрат метілтрансфсра- зами. Відомо кілька ферментних систем, що каталізують A-метилювання природних і чужорідних амінів. Фенілетаноламін-А-метілтрансфе- рази каталізує утворення адреналіну з норадреналіну і А-метілірова- ня інших фенілетаноламінових похідних.
Катехоламінові гормони, а також ряд чужорідних сполук, таких, як галова і кавова кислоти, метіліруется катехол-О-метилтрансферазою. Для реакції потрібно S-аденозилметионин як метилового донора, а також Mg2+ або інші двовалентні іони.
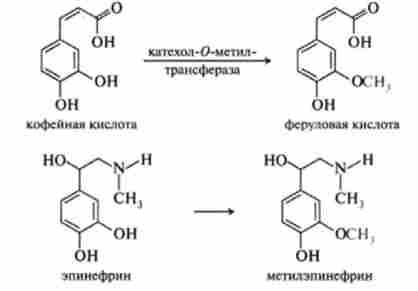
при S-метилировании метильние групи переносяться до тіоловим групам чужорідних сполук, таких, як метил і етил меркаптани, меркапто- етанол і ін.
ацетилювання - це основний шлях метаболізму ароматичних амінів, сульфамідів і деяких чужорідних ароматичних амінокислот. Ацетилювання зазвичай вважають функцією печінки, однак у кроликів ацетилювання сульфаниламида і ля / ю-амінобензойної кислоти відбувається в ретикуло- ендотеліальних клітинах селезінки, а не в печінці.
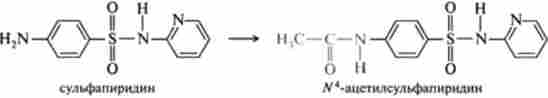
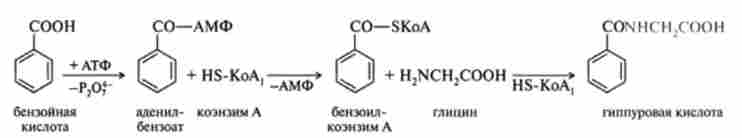
кон'югація з гліцином і іншими амінокислотами є характерною метаболічної реакцією ароматичних карбонових кислот, таких, як бензойна і гетероциклічні карбонові кислоти. Механізм пептидного кон'югації полягає в освіті коензим-А-похідних чужорідних карбонових кислот, які взаємодіють з гліцином. В результаті утворюється гиппуровая кислота і виділяється вільний коензим А:
Реакції другої фази біотрансформації локалізовані в різних ком- партментах клітин. Дані представлені в табл. 32.3.
Підсумовуючи основні положення метаболізму ксенобіотиків в організмі, можна відзначити наступні основні моменти.
- Реакції біотрансформації є ферментативні перетворення ліпофільних, чужорідних і деяких ендогенних речовин в організмі.
Таблиця 32.3. Найбільш важливі реакції другої фази біотрансформації в залежності від локалізації і дії на субстрати
|
Тип реакції |
локалізація |
ендогенний субстрат |
|
Освіта глкжуронідов |
ендоплазматичнийретикулум |
Гормони шітовідной і пазових залоз |
|
Сульфирование |
цитозолем |
Стероїди, карбогідрати |
|
ацетилювання |
цитозолем |
Карбогідрати. серотонін |
|
метилирование |
цитозолем |
біогенні аміни |