| Головна |
| «« | ЗМІСТ |
|---|
глутамінова кислота (Глутамат) забезпечує передачу збудження але Длінноаксонние волокнам, а нейронів з такими аксонами в ЦНС понад мільйон. Безліч сенсорних волокон, що несуть в ЦНС зорову, слухову, тактильну, больову інформацію, є глутаматергічних. Те ж саме можна сказати і про більшість асоціативних шляхів, що зв'язують між собою відділи мозку. Передача самої інформації, як еферентної, так і афферентной, здійснюється за рахунок медіаторів, що відносяться до збудливим амінокислотам, а модуляція цієї передачі відбувається за рахунок гальмівних амінокислотних медіаторів (ГАМК, гліцину). Ацетил холін і біогенні аміни тим часом контролюють рівень неспання, а також рівень емоцій. Ще більш повільні регуляторні впливу на роботу мозку надають гормональні впливу регуляторних пептидів.
Глутамат - харчова амінокислота; людина споживає її в кількості 5-10 г / сут. Однак вона, як і належить медіаторів, не проходить з крові в тканини мозку, затримуючись гематоенцефалічний бар'єр (ГЕБ). В якості медіатора вона заново синтезується в пресінаітічних закінченнях нейронів з глутаміну (рис. 9.16, а), А після викиду в синаптичну щілину і взаємодії з рецепторами захоплюється гліальними клітинами (астроцитами), перетворюється в глутамин, аспарагінову кислоту і ГАМК. Глутамин знову надходить в нейрони для синтезу з нього глутамату (рис. 9.16, 6).
аспарагінова кислота (Аспартат) за своїми властивостями близька до глутамату та взаємодіє з його рецепторами. Аспартат є медіатором в збудливих інтернейронах в спинному і середньому мозку. При деполяризації мембрани нервового закінчення глутамат викидається з везикул в щілину і може зв'язатися з рецепторами на постсинаптичні мембрані. Описано понад 10 типів рецепторів до глутамату, що розрізняються і за механізмом передачі сигналу, і але розташуванню в ЦНС. Ці рецептори можуть бути метаботропнимі і іонотропнимі (див. Схему):

Серед метаботропних рецепторів виділяють ACPD-tvui, що активується амінодікарбоксіціклопентаном (APCD). Інші різновиди рецепторів, що передають сигнал, пригнічуючи активність АЦ або активуючи фосфо інозітольную систему (ІФ3, ДАГ) і збільшуючи концентрацію кальцію в клітині, але не активуються ACPD, назвали «не-АСРП ».
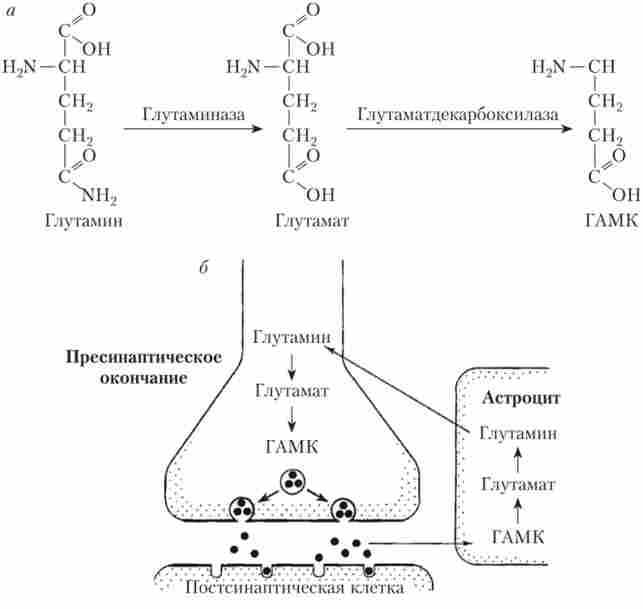
Мал. 9.16. Обмін глутамінової кислоти в ЦНС:
а - шлях біосинтезу в пресинаптичному закінчення;
6 - метаболізм ГАМК та глутамату за участю астроцити
Метаботропние глутаматние рецептори широко представлені в мозку. Вони беруть участь у формуванні механізмів болю, тривожності, пам'яті, а також в нейродегенеративних процесах.
Іонотронние рецептори до глутамату поділяються на два підтипи - NMDA (активується NMDA - М-метил-Л-аснартатом) і не-NMDA. IIe-NiWZM-підтип поширений по всьому мозку і підрозділяється на дві групи: каінатние (активуються каїнової кислотою) і АМРА (активуються АМРА - а-аміногідроксіметілізоксанолпропіоновой кислотою). У кожному з цих підтипів в свою чергу є по кілька різновидів рецепторів, і вони можуть розташовуватися і пресіптічно, і постсинаптично.
При порушенні постсинаптичних ЛМРЛ-рецепторів відкриваються канали для іонів натрію і кальцію, що сприяє швидкій деполяризації мембран і порушення цієї клітини. При активації пресінап- тичних НЕ-МШЕЛ-рецепторів іони Са2+ входять в пресинаптичне закінчення, що забезпечує вивільнення медіатора з закінчення в синаптичну щілину.
Каінатние рецептори локалізовані переважно на закінченнях нейронів, що вивільняють глутамат, і при їх порушенні збільшується викид цього медіатора. Таким чином, не-ЛгМОЛ-рецептори відіграють важливу роль в регуляції пластичності синаптичної передачі. Штучні агоністи каінатного рецепторів дозволяють створити нові лікарські засоби, що активують глутаматних систему.
iVMZM-рецептори повсюдно поширені в мозку ссавців. Як і ЛМРЛ-рецептори, вони розташовуються іресінаптічно і постсинаптично. Висока їх щільність виявлена в гіпокампі, таламусі, базальних гангліях, корі великих півкуль.
ЛгМ?) Л-рецеітори утворюють неспецифічні катіонні канали, щоб забезпечити проходження іонів К+, Naf і Са2 '. На відміну від нc-NMDA- рецепторів, викликають швидку деполяризацію, активація NMDA- рецепторів призводить до пролонгованої деполяризаціїмембрани, що створює основу для тривалої потенциации в гіпокампі.
NMDA-рецептор утворений чотирма білковими субодиницями, на яких є два місця для зв'язування глутамату і два місця для зв'язування гліцину. Ці ж субодиниці, пронизуючи біліпідний шар мембрани, утворюють катіонний канал, який при ПП на мембрані перекритий іоном Mg2+ і, природно, нічого пропускати не може (рис. 9.17).
Для того щоб перевести iVMD / 1-канал в робочий стан, необхідно деполярізовать мембрану в області каналу до -40 мВ за рахунок якихось інших рецепторів, а також необхідна присутність амінокислоти гліцину. Сам по собі гліцин не викликає відкриття каналу рецептора, а діє, потенціюючи ефекти глутамату. Якщо в середовищі присутня гліцин, і він може зв'язатися своїми активними центрами на NMDA-рецепторі, то невелика деполяризація може бути забезпечена в тому випадку, якщо глутамат діє на розташовані поблизу від NMDA-рецептора якісь інші ne-iVMZM-рецептори. Вважається, що це можуть бути рецептори підтипу АМРА. При такій деполяризації магнієва пробка вибивається, гліцин і глутамат, взаємодіючи зі своїми місцями зв'язування, відкривають канал NMDA - ре це1 пора, і в клітку почнуть надходити натрій і кальцій (див. рис. 9.17). Описаний механізм лежить в основі так званої
довгострокової потенциации - одного з механізмів короткочасної пам'яті.
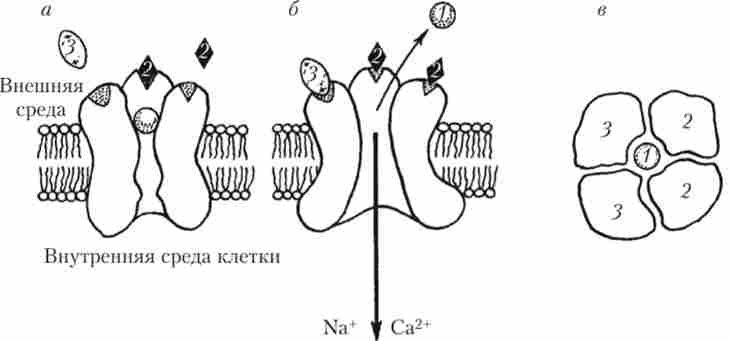
Мал. 9.17. Схема роботи домол-рецепторів:
а - NMDA-рецептор инактивирован, канал рецептора закритий; 6 - мембрана деполяризована до -40 мВ, NMDA - рецептор активований, канал відкритий; в - розріз поперек осі каналу инактивированного NMDA-рецептора; 1 - іон Mg2+;
2 - глутамат; 3 - гліцин; одна з чотирьох білкових субодиниць з місцем зв'язування для гліцину НЕ зображена
Вхід в нейрон натрію і кальцію через NMDA-кттл повинен строго регулюватися, так як надлишок кальцію активує роботу багатьох ферментативних систем клітини, що може привести до надмірного збудження, пошкодження і навіть загибелі нейрона. Це явище отримало назву глутаматной токсичності, і спостерігається воно рідко, так як глутамат практично не проникає з крові в мозок. Глутамат значно загострює чутливість всіх смакових рецепторів, і без нього їжа здається прісною і несмачною.
Малі дози глутамату і його агоністів застосовуються в клініці: але 2-3 г глутамату на добу при виснаженні 11C. Типовим наслідком введення агоністів глутаматних рецепторів є помітна активація ЦПС - аж до розвитку судом. Особливо відома в цьому сенсі каїнова кислота - токсин однією з діатомових водоростей, що викликає у великих дозах дегенерацію глутаматергічних нейронів.
Антагоністи №ШХ4-рецепторів використовуються у випадках, коли потрібно знизити збудливість мозку: при судомах, безсонні, підвищеної тривожності, больових синдромах. Однак ефекти цих антагоністів носять занадто широкий характер і їх небезпечно приймати без спостереження лікарів. «Пробкові» блокатори №ШХ4-рецепторів, наприклад калипсол (кетамін), мають сильний аналгетичний ефект, але викликають галюцинації. Ще більш сильний анальгетик цього класу - фенциклидин, що володіє рядом психотропних ефектів і часто викликає спалахи агресивності, причому нейтралізувати хворого важко, так як він зовсім не відчуває болю і страху.
АТФ і споріднені з ними сполуки відносяться до хімічних сполук класу пуринів. Виявилося, що і аденозин, і його похідні є медіаторами і в ЦНС, і в периферичної НС (рис. 9.18).
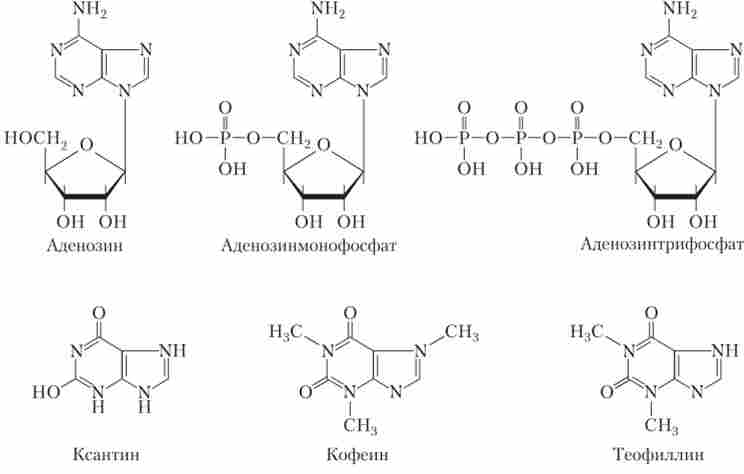
Мал. 9.18. Ліганди пуринових рецепторів
Рецептори до пуринів поділяють на два класи: Р ,, що відрізняються найбільшою чутливістю до аденозину, і Р2, найбільш чутливі до АТФ. У свою чергу, рецептори Р, і Р2 ділять на підкласи (табл. 9.2). Метаботропние рецептори - РАХ, Р ^ А2. іонотропние рецептори - Р2Х, Р2 У.
Таблиця 9.2
пуринергічні система
|
рецептор |
р 1 |
Р2 |
||
|
медіатор |
аденозин > АМФ > АДФ > АТФ |
АТФ > АДФ > АМФ |
||
|
підтип |
Ml |
М2 |
Р2Х |
Р2У |
|
підвиди |
2 підвиду |
2 підвиду |
7 підвидів |
15 підвидів |
|
передача сигналу |
метаботропние |
метаботропние |
Катіонні ліганд-активи- руемой канали |
іонотропние |
|
Придушення АЦ 1 |
Активація АЦТ |
Посилення входу кальцію і натрію в клітку |
Активація Фос фоінозіголь- ної системи: вхід Са2+ до клітки |
|
|
рецептор |
р2 |
|||
|
антагоністи |
Ксантини (кофеїн, теофілін) |
хінідин |
||
|
Дія агоністів |
Нейропротекция при шоці, крово- втрати. Гальмування НА-, 5-НТ- і глутаматной систем, гальмування збудження, седативний ефект. Анальгезия. Ангісудорожное дію |
Активація Д2- дофаминовой системи. Розширення артерій, зниження згортання крові |
Активація глутаматной системи. Звуження судин. Антагоністи пригнічують біль і запалення |
Розширення судин, посилення згортання крові |
Найчастіше рецептори до пуринів розташовані на постсинаптичних мембранах, як в мозку, так і в периферичних тканинах: гладких м'язах судин, бронхів, кишечника, м'язі серця, тромбоцитах. Аденозин частіше є самостійним медіатором, а АТФ нерідко зустрічається в одних і тих же закінченнях з іншими медіаторами - НА, АХ, будучи їх комедіатором.
При високих енергетичних затратах відбувається інтенсивне утворення АМФ з АТФ, а АМФ є одним з основних природних лігандів Р]А]-рецепторів. Тому при виснаженні енергетичних систем мозку відбувається вплив АМФ на ці рецептори і включення через них цілого комплексу захисних механізмів, що характеризуються зниженням активності більшості медіаторних систем мозку, седативну і снодійним ефектом. антагоністи рецепторів Р{А{ і, в меншій мірі, РА2 є за своєю хімічною природою ксантинами, і ми зустрічаємося з ними постійно. Це діючий початок кави (кофеїн) і чаю (теофілліі), що блокують сильніше РАХ- і, в меншій мірі, Р1А2-рецептори. Ось чому не варто пити міцні каву і чай на ніч. Однак у значної кількості людей високою чутливістю до ксантину врожденно присутні Р1Л2-рецептори, що активують нервову систему, і їх придушення призводить до снодійним ефектів. При вживанні високої концентрації різних ксантинів людина відчуває оглушення, дезорганізацію поведінки і т. П. Хоча відомо, що вживання розумних кількостей кави (одну-трьох маленьких чашок в день) є одним з кращих способів профілактики такого страшного вигляду старечого недоумства, як хвороба Альцгеймера. Інозин - метаболіт аденозину, - взаємодіючи з пуриновими рецепторами обох класів, розширює коронарні судини серцевого м'яза, збільшує силу серцевих скорочень. На основі аналога аденозінолітіка теофіліну (трентал) отримано ліки для поліпшення мікроциркуляції крові, наприклад, в мозку, оці і т. П.
гістамін синтезується з харчової амінокислоти гістидину та присутня в більшості тканин, хоча його розподіл в організмі дуже нерівномірно (рис. 9.19).

Мал. 9.19. біосинтез гістаміну
У мозку гістамін є медіатором, але тіла нейронів, що містять гістамін, зібрані дуже компактно в туберомаммілярном ядрі заднього гіпоталамуса. Гістамінсодержащіе нейрони сильно розгалужуються, і їх волокна виявлені практично у всіх відділах мозку. Часто замість пресинаптичних закінчень гістамін виділяється прямо по ходу волокна, досягаючи не тільки нервових клітин, але і гліальних клітин і клітин судин.
У периферичних тканинах гістамін зосереджений головним чином в лейкоцитах і в гранулах тучних клітин. У доглянутому вигляді гістамін неактивний, але багато впливу призводять до його викиду і провокують сильні фізіологічні ефекти. Найбільше огрядних клітин, а отже, і гістаміну, знаходиться в місцях, де найбільш імовірні потенційні пошкодження організму: в шкірі, в носі, в роті, на стопах, а також на внутрішніх поверхнях організму, біля місць розгалуження кровоносних судин. До теперішнього часу описано три види рецепторів до гістаміну: TIV Н2 і #3, всі вони метаботропние (табл. 9.3).
Таблиця 93
гістамінові рецептори
|
підтипи рецепторів |
", |
н2 |
"з |
|
локалізація |
Постсинаптичні: бронхи, судини, нейрони, глия |
Постсинаптичні: шлунок, кишечник, матка |
Пресинаптичні: НС (стриатум, чорна субстанція, лобові частки кори) |
|
передача сигналу |
Активація Фос фоінозітольной системи (ІФ3, ДАГ) |
Активація АЦТ |
придушення alU |
|
антагоністи |
Димедрол, сунрастін |
Циметидин, ранітидин |
Тіоперамід |
|
підтипи рецепторів |
я, |
н2 |
Я3 |
|
ефекти антагоністів |
Загальне збудження, підвищення тривожності, аналгезія, зниження апетиту, підвищення сексуальної активності |
Секреція шлункового соку, посилення перистальтики кишечника, скорочення матки, стимуляція імунітету, посилення агресивності |
Регуляція (частіше гальмування) викиду різних медіаторів, в тому числі гістаміну, НА, Д, 5-НТ, АХ |
рецептори типів Н{ і #2 розташовані постсинаптично, але перші частіше зустрічаються в межах мозку, а другі - в периферійних органах. #3-тип рецепторів, вивчений поки гірше інших, відрізняється пресінапті- чеський локалізацією в межах ЦНС і дуже високою чутливістю до гістаміну. Всі рецептори до гістаміну - метаботропние, і ефекти опосередковані через G-білки. але через Н{ активується фосфоінозітоль- ная система, через Н2 активується АЦ, а через #3 АЦ пригнічується.
Як протиалергічних засобів широко використовуються анти- гистаминние препарати, що прискорюють руйнування гістаміну або блокують Яртіп рецепторів. блокатори Я2-рецепторів успішно застосовують в клініці при виразковій хворобі, викликаної надмірною секрецією соляної кислоти в шлунку.
Гістамін бере участь в місцевій регуляції кровотоку: при нестачі кисню в будь-якої тканини, там локально підвищується рівень гістаміну, миттєво розширюючи капіляри і покращуючи мікроциркуляцію крові.
Значна роль належить гістаміну в забезпеченні такої важливої захисної реакції, як запалення, при якому також потрібно різко посилити кровообіг в ураженому місці. Гістаміном можна отруїтися, вживаючи в їжу м'ясо тунця або макрелі, так як в тканинах цих риб дуже швидко накопичується гістамін, що утворюється з гістидину при неправильному зберіганні. При отруєнні дуже швидко розвивається прилив крові до обличчя, починаються нудота, біль в шлунку, на шкірі з'являється кропивниця.