| Головна |
| «« | ЗМІСТ | »» |
|---|
медіатори (Трансмітери) - фізіологічно активні речовини, безпосередньо передають інформацію від однієї клітини до іншої через спеціальні міжклітинні контакти - синапси.
На периферії медіаторами найчастіше служать два речовини - АХ (нервово-м'язові синапси і синапси парасимпатичного відділу ВНС) і НА (синапси постгангліоіарних волокон симпатичного відділу ВНС). Але в ЦНС збудження і гальмування можуть передаватися з нейрона на нейрон за допомогою багатьох медіаторів. Серед збуджуючих медіаторів найчастіше зустрічаються глутамат, АХ, НА, Д, серотонін, а серед гальмівних - ГАМК і гліцин. Але є і досить рідко зустрічаються хімічні посередники, що виробляються в відносно малому числі нервових клітин. Вважають, що медіаторами в нашому мозку є не менше 35-40 різних речовин. Саме порушення у виробленні або утилізації медіаторів є основною причиною безлічі нервових і психічних розладів.
Властивості речовини, здатного стати медіатором, представлені на рис. 9.4.
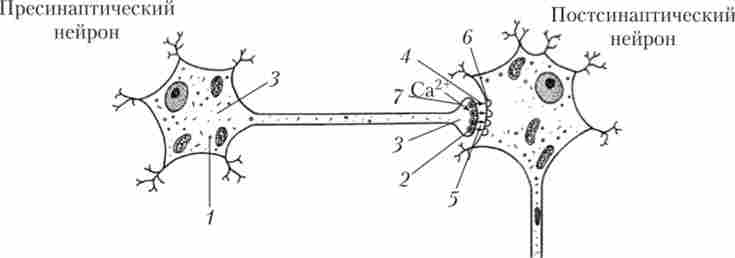
Мал. 9.4. Вимоги до потенційного медіатора:
1 - медіатор і його хімічні попередники повинні бути присутніми в нейроні; 2 - медіатор повинен міститися в високих концентраціях в синаптичних везикулах; 3 - в синаптичному закінчення і (або) в тілі нейрона повинна міститися ферментативна система синтезу медіатора; 4 - медіатор повинен вивільнятися з везикул в синаптичну щілину при приході ПД до нервового закінчення; 5 - викиду медіатора в синаптичну щілину при стимуляції повинен передувати вхід в закінчення іонів кальцію; 6 - в синаптичної щілини повинна бути присутнім система деградації медіатора і (або) система його зворотного захоплення в пресинаптичне закінчення; 7 - на постсинаптичні мембрані повинні бути присутніми рецептори до медіатора
за своєю хімічною природою медіатори можна поділити на «класичні», Що є видозміненими амінокислотами, і«некласичні»- пептидні і газоподібні (табл. 9.1). Традиційно медіатори ІА і Д, синтезовані в організмі з харчової амінокислоти фенілаланіну, що містить катехоловое ядро, називають катехоламинами. Серотонін, який синтезується з амінокислоти триптофану і за своєю хімічною природою представляє собою похідне індолу, разом з НА та Д відносять до групи біогенних амінів, хоча і серед інших медіаторів зустрічається безліч «амінів».
Таблиця 9.1
Деякі медіатори, виявлені в організмі тварин
|
Тип |
Назва |
|
«Класичні» збуджуючі |
Ацстілхолін, НА, Д, серотонін, глутамат, гістамін, пурини (АТФ, АДФ, аденозин) |
|
«Класичні» гальмівні |
ГАМК, гліцин |
|
пептидні |
субстанція Р нейропептид Y, еікефаліни, еідорфііи і ін. |
|
газоподібні |
N0, СО, H, S |
За своїм ефектам класичні медіатори поділяють на збуджуючі і гальмівні. Багато пізніше «класичних» медіаторів були відкриті пептидні медіатори, що представляють собою невеликі ланцюжки з амінокислот. Доведено медіаторная роль кількох пептидів, і кілька десятків пептидів знаходяться «під підозрою». І нарешті, досить несподіваним було виявлення здатності клітин виробляти ряд газоподібних речовин, для секреції яких не потрібні «упаковка» в везикули; проте вони є повноцінними медіаторами. Краще за інших газів в ролі медіатора відомий оксид азоту (NO), але медіаторні властивості СО і H2S також не викликають сумнівів.
Будь-медіатор, незалежно від хімічної або фізичної природи, має свій життєвий цикл, що включає наступні етапи:
Синтез медіаторів може відбуватися як в тілі нейрона, так і в самих пресинаптичних закінченнях. Молекули медіаторів пептидної природи ферментативно «вирізаються» з великих білків-попередників, які синтезуються в тілі нейрона на шорсткою ЕПР. потім ці
медіатори упаковуються в апараті Гольджі в великі везикули, які за допомогою аксонального транспорту рухаються але аксону до синапсах. «Класичні» медіатори синтезуються в самому кінці його, куди ферменти для синтезу і упаковки молекул в везикули надходять за рахунок аксонального транспорту. У більшості нейронів домінує якийсь один медіатор, проте в останні роки встановлено, що в одному і тому ж нейроні і, більш того, в одному і тому ж синапсі можуть бути присутні кілька медіаторів. Вони можуть перебувати як в одних і тих же, так і в різних везикулах. Таке співіснування показано, наприклад, для біогенних амінів і пептидних медіаторів.
Викид медіатора в синаптичну щілину відбувається в той момент, коли ПД досягає нервової терміналі і пресинаптична мембрана деполяризуется (рис. 9.5).
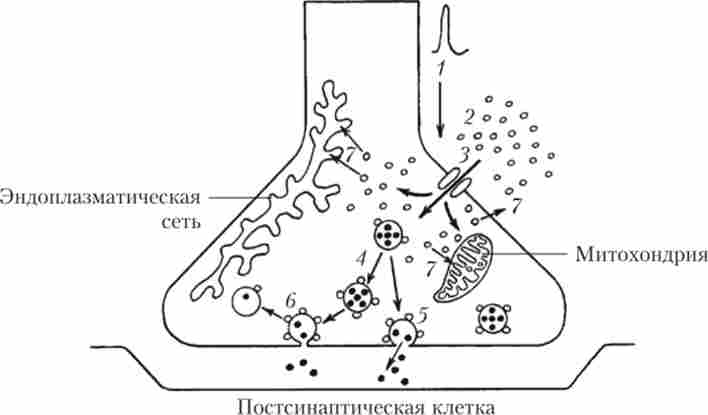
Мал. 9.5. Передача збудження через хімічний синапс:
У цей момент в мембрані відкриваються потенціалзалежні кальцієві канали і Са2+ входить в пресинаптичне закінчення, зв'язуючись з певним білком на зовнішній стороні мембрани везикул і запускаючи процес злиття везикули і пресинаптичної мембрани. Везикула може, по-перше, вбудуватися в неї цілком і «викинути» весь свій вміст в синаптичну щілину ( «повне злиття»). По-друге, може утворюватися короткостроковий контакт ( «пора злиття») зі спеціальних білків між мембраною везикули і мембраною закінчення. Через пору злиття частина молекул медіатора встигає вийти в синаптичну щілину (такий спосіб секреції медіатора називається «kiss-and-run»(В перекладі з англ,« цілуй і біжи »).
Як тільки медіатор виявився в щілини, необхідно дуже швидко прибрати увійшов в нервове закінчення кальцій. Для цього існують спеціальні зв'язують кальцій білки-буфери, а також кальцієві насоси, що відкачують кальцій в ендоплазматичну мережу, в мітохондрії і в зовнішнє середовище. В цей час спустошені (kiss-and-run) Або заново формуються в нервовому закінченні везикули знову наповнюються молекулами медіатора.
Потрапили в синаптичну щілину молекули медіатора досягають постсинаптичної мембрани за рахунок дифузії і взаємодіють з рецепторами. Традиційно терміном «рецептор» позначаються спеціальні клітини або клітинні чутливі освіти, що реагують на подразники зовнішнього і внутрішнього середовища: фоторецептори, механорецептори і т. П. У сучасній біології термін «рецептор» вживають також по відношенню до молекул білків, вбудованих в клітинну мембрану або перебувають в цитоплазмі і здатних реагувати зміною своєї форми і стану па специфічні для кожного виду рецепторів впливу. Рецептори знайдені для медіаторів, гормонів, антитіл та інших сигнальних молекул, важливих для передачі інформації в живих системах.
Передача сигналу через мембрану включає в себе три стадії:
виділяють два основних види рецепторів - іонотропние (канальні) і метаботропние.
прикладом канального рецептора може служити ліганд-активується (хемочувствітельності) рецептор для АХ, що розташовується на мембрані волокон скелетних м'язів (див. рис. 8.17). Такі рецептори крім природного АХ активуються алкалоїдом тютюну - нікотином. Тому їх називають нікотиновими або Н-холинорецепторами. Крім поперечно-смугастих м'язів такі рецептори зустрічаються і в ЦНС. Канал складається з п'яти білкових субодиниць, зібраних в своєрідну трубку, пронизливий мембрану наскрізь. Дві субодиниці однакові і позначаються а. Коли дві молекули медіатора АХ приєднуються до спеціальних місцях зв'язування на а-субодиниць, канал відкривається для катіонів Na+ і Са2+ (Рис. 9.6).
В результаті на постсинаптичні мембрані розвивається ВПСП, і клітина може збудитися. Взаємодія медіатора з рецептором триває 1-2 мс, а потім молекула медіатора повинна від'єднатися, інакше рецептор «втратить чутливість» і тимчасово перестане реа-
гірованного на нові порції медіатора. Канальний вид рецепції дуже швидкий, проте він зводиться або до деполяризації постсинаптичної клітини за допомогою відкриття катіонних каналів, або до се гіперполяризації шляхом відкриття хлорних каналів.
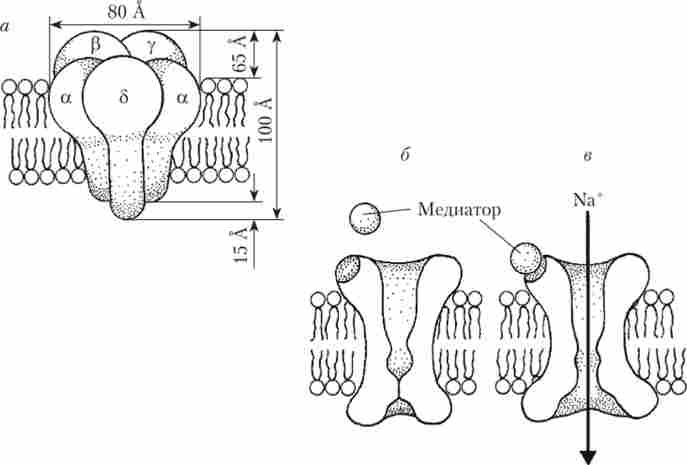
Мал. 9.6. Модель будови нікотинового холінорецептора:
а - схема будови; 6 - капа.;: закритий; в - канал відкритий; А - ангстрем (1СГ10 м)
метаботропние рецептори являють собою молекули білків, які сім разів «пропущені» через клітинну мембрану, утворюючи три петлі всередині клітини і три - на зовнішній стороні клітинної мембрани (рис. 9.7).
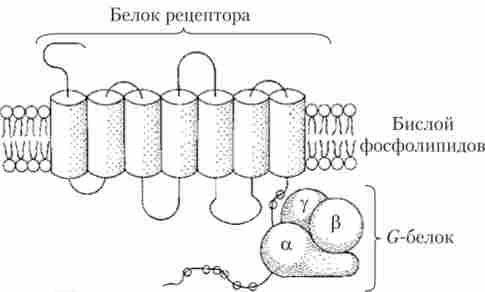
Мал. 9.7. Метаботропних рецептор, пов'язаний з G-білком:
а, р, у - субодиниці G-бел ка
В даний час виявлено безліч подібних рецепторних білків, причому частина білкової молекули, звернена всередину клітини, пов'язана з відповідним G-білком. G-білки отримали свою назву за здатність розщеплювати ГТФ (гуанозинтрифосфат) до ГДФ (гуанозиндифосфат) і залишку фосфорної кислоти. Ці білки складаються з трьох субодиниць: а, р, у (див. Рис. 9.7), причому відомо кілька підтипів а-субодиниць. Той чи інший підтип а-субодиниць, що входять до складу G-білка, визначає, на який процес в клітці буде впливати даний G-білок. Наприклад, Gj.-білок (т. Е. Включає в себе а5-субодиницю) стимулює фермент АЦ, Gq стимулює фосфоліпазу С, G0 зв'язується з іонними каналами, Gj гальмує активність АТ. Часто один різновид G-білка впливає на кілька процесів в клітині. За відсутності ліганду (медіатора або гормону), який може зв'язатися з метаботропних рецептором, G-білок неактивний. Якщо ж з рецептором зв'язався відповідний йому активує ліганд - а-субодиниця активується (ГДФ заміщується на ГТФ), від'єднується від комплексу субодиниць Ру і короткий час взаємодіє з білками-мішенями, запускаючи або, навпаки, гальмуючи внутрішньоклітинні процеси. Субодиниці G-білка не можуть існувати окремо протягом довгого часу і після гідролізу ГТФ а-суб'едіііцей утворюють єдиний неактивний G-білок. Діючи на цілий ряд ферментів і іонних каналів, активовані G-білки запускають каскад внутрішньоклітинних хімічних реакцій, в результаті яких змінюється концентрація низки регуляторних молекул - вторинних посередників (Первинні посередники - молекули, які переносять сигнал від клітини до клітини, м. Тобто медіатор, гормон).
До найбільш поширених вторинним посередникам (мессенджерам) відносять цАМФ, який утворюється з АТФ під дією ферменту АЦ. Якщо ж в результаті впливу ліганда на рецептор активується G ^-форма білка, то вона активує фермент фосфоліпазу С, яка в свою чергу стимулює утворення з фосфоліпідів мембран двох посередників: ІФ3 (Інозітолтріфосфат) і ДАГ (діацілгліцерола). Обидва посередника призводять до збільшення в клітці концентрації кальцію за рахунок його надходження ззовні (через іонні канали) або при викиді його з внутрішньоклітинних депо. Са2+ - найпотужніший внутрішньоклітинний стимулятор процесів життєдіяльності клітини. Крім того, ІФ3 і ДАГ стимулюють ріст клітин, сприяють експресії генів, вивільненню медіаторів, секреції гормонів і т. п. Однак вторинний посередник прямо або через ряд проміжних стадій впливає на хемочувствітельності іонні канали - відкриває або закриває їх. Це сприяє розвитку збудження або гальмування клітини, в залежності від того, які канали зазнали впливу. Величина і тривалість потенціалів буде залежати від виду, кількості та часу взаємодії молекул медіатора з рецепторами, а в підсумку - від того, яка система вторинних посередників активується під дією медіатора.
Характерною рисою метаботропних рецепції є її каскадність, що дозволяє багаторазово посилити вплив медіатора на клітку (рис. 9.8).

Мал. 9.8. Принципова схема каскаду шляхів передачі сигналу після впливу ліганда на метаботропних рецептор
Як вже говорилося, медіатор не повинен взаємодіяти з іонотропних або метаботропних рецептором довше 1-2 мс. У нервово-м'язових синапсах АХ дуже швидко руйнується ферментом ацетилхолінестеразою до холіну і ацетату. Утворився холін транспортується в пресінап- тичне закінчення і знову використовується для синтезу АХ. Аналогічно руйнуються відповідними ферментами в синаптичної щілини і інші медіатори (АТФ, пептиди).
Інший поширений варіант усунення медіатора з синаптичної щілини - це його зворотне захоплення (англ, reuptake) В пресинаптичне закінчення або в гліальні клітини. НА, Д і серотонін після захоплення закінченнями знову «пакуються» в везикули або можуть бути зруйновані внутрішньоклітинними ферментами. ГАМК і глутамат транспортуються з синаптичної щілини в клітини глії і, зазнавши ряд біохімічних перетворень, знову потрапляють в нервові закінчення.
В процесі еволюції природа створила безліч фізіологічно активних речовин, що діють на метаболізм медіаторів. Багато таких речовин виробляють рослини з метою захисту. Разом з тим, отрути, що діють на життєвий цикл медіаторів і синаптичну передачу, виробляють деякі тварини: для нападу на жертву або для оборони від хижаків.
Величезна кількість хімічних сполук, що впливають на роботу медіаторних систем, створюється штучно людиною в пошуках нових лікарських засобів, що впливають на функціонування НС.