| Головна |
| «« | ЗМІСТ | »» |
|---|
Існує кілька принципів класифікації моносахаридів:
В основу номенклатури цукрів покладені тривіальні назви моносахаридів складу ЗяН2лПроя з прямою ланцюгом вуглецевих атомів: ксилоза, рибо-за, глюкоза, фруктоза і ін. найменувань кетоз надається закінчення -улоза, наприклад кетоза З5-пентулоза. Всім моносахаров властива конфігураційна (оптична) ізомерія, т. Е. Вони існують в двох енантіомерний формах: DHL. Належність моносахаридів до D- або L-ряду визначається по розташуванню ОН-групи у останнього (рахуючи від альдегідної або кетогруп- пи) хірального атома вуглецю. Як стандарт порівняння конфігурації асиметричного атома вуглецю запропоновано використовувати ізомер гліцеринового альдегіду. Названий D-гліцериновим альдегідом ізомер обертає площину поляризованого світла вправо, а його дзеркальне відображення антипод - L-гліцериновий альдегід - вліво:

Всі моносахариди, які теоретично можуть бути отримані з D-гли- церінового альдегіду шляхом послідовного подовження його ланцюга з боку альдегідної групи, називають D-цукрами, незалежно від змін інших атомів вуглецю, а отримані таким же способом з L-гліцеріно- вого альдегіду - L-цукрами:
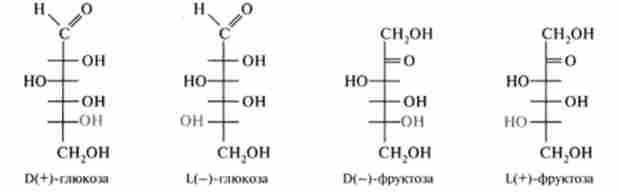
Деякі моносахариди, наприклад фруктоза, віднесені до D-ряду, є левовращающімі, а представники L-ряду - правовращающих. Щоб вказати і приналежність цукру до D- або L-ряду, і напрямок обертання площини поляризації, після символів D або L перед назвою моносахарида в дужках ставлять знак (+) або (-), що позначає відповідно праве або ліве обертання.
В живих організмах моносахариди присутні переважно в D-конфігурації, яку називають природною. Виняток становить L-арабиноза бактерій, L-Рамноза і L-сорбоза рослин.
Нижче наведені стереохимичні співвідношення D-альдоз і D-кетоз, що містять від С-3 до С-6 вуглецевих атомів:
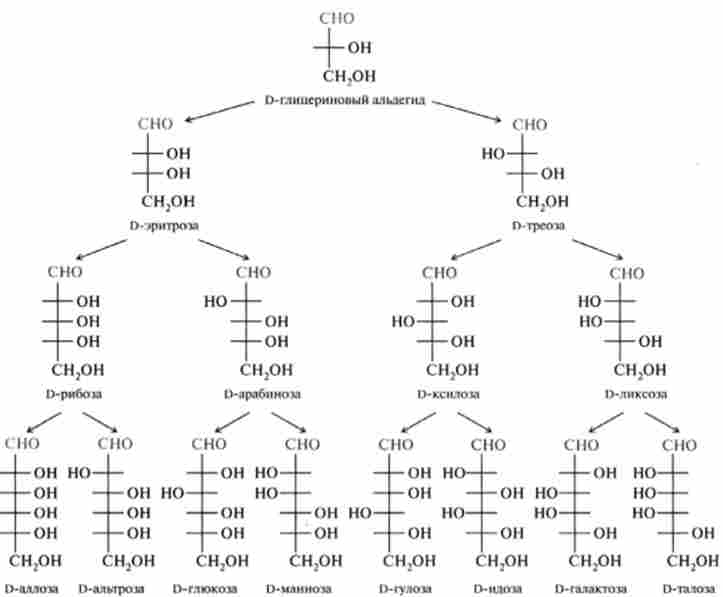
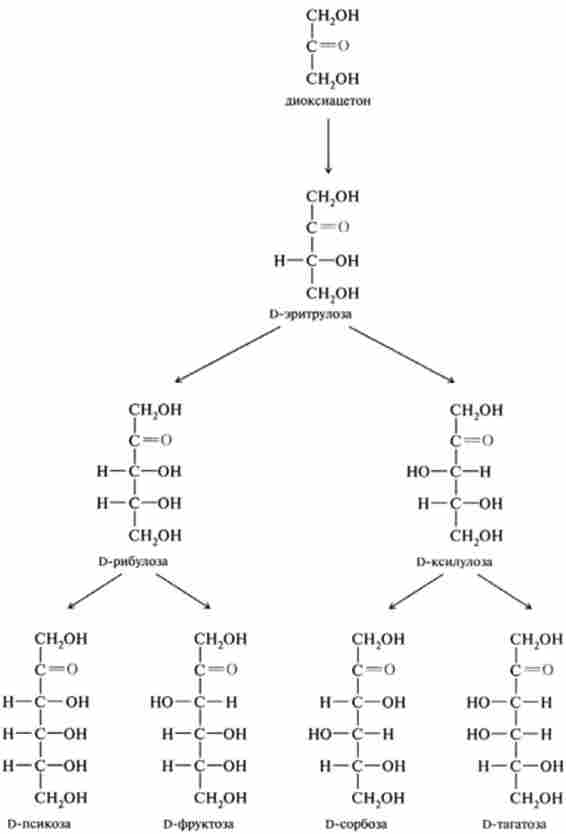
У альдоз, починаючи з п = 4, і кетоз - з п = 5 є кілька хіральних центрів, т. Е. Існує ряд діастереомерів, що представляють собою різні за хімічним властивостям з'єднання, причому кожен з діастереомерів може існувати в L- і D- конфігурації. Так, число стереомеров альдогексоз з чотирма хіральними центрами дорівнює 24, т. е. шістнадцяти. Останні можна згрупувати в вісім пар енантіомерів в D- і L-ізомери, що мають однакові хімічні і фізичні властивості і відрізняються тільки напрямком обертання площини поляризованого світла.
Карбонільні групи моносахаридів з довжиною ланцюга п = 5 і більше можуть вступати у взаємодію зі спиртовими групами з утворенням циклічної напівацеталі, або полукеталі, які називаються відповідно фура
нічними або піраночнимі за аналогією з відомими сполуками - фура- ном або піраньї:
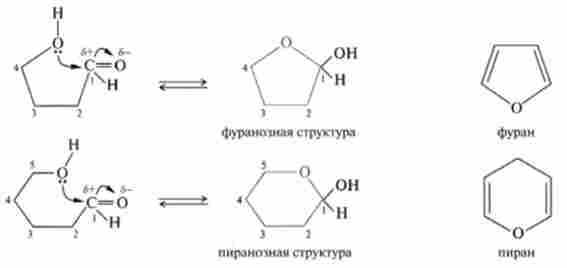
При цьому в молекулі пентоз або гексоз з'являється еше один хіральний центр і нова пара ізомерів - а- і p-аномери, що відрізняються розташуванням гідроксильної групи при полуацстальном атомі вуглецю відносно площини кільця: у а-аномери гидроксильная і СН2ОН-групи знаходяться по різні площини кільця, а у p-аномери - по одну його сторону. Таким чином, гексоза утворює чотири циклічні форми (а- і p-фуранозной і а- і р-пі-ранозную), що знаходяться в розчині в динамічній рівновазі з ацикличної формою. У водному розчині всі ці форми здатні взаємно перетворюватися один в одного через оксоформу (нециклічних форму) глюкози, кількість якої становить менше 1%.
Нижче наведені взаємоперетворення різних форм глюкози у водному розчині:
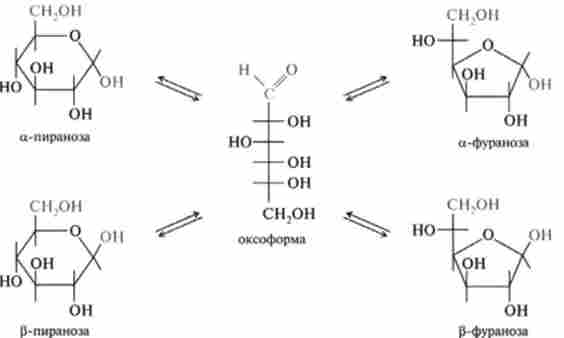
Пиранозного форми гексоз і пентоз значно більш стійкі, ніж виженіть- ранозние, тому в розчині завжди істотно переважають перші, а- і Р-Форми моносахаридів, що володіють різною величиною оптичного обертання, в процесі розчинення у воді взаємно переходять одна в одну, тому питоме обертання (a]D в свіжоприготовлених розчинах моносахаридів змінюється протягом часу до певної величини. Це явище отримало назву муторотаціі (Від лат. multirotatia - багато обертань). Так, при розчиненні у воді a-D-глкжози ([а] р = + 112,2 °) і p-D-глюкози (1а] Р = + 18,7 *) питоме обертання змінюється до встановлення рівноваги (36% а-форми, 64% [3-форми і сліди нециклічного форми), в момент якого воно досягає + 52,7 °.
В даний час для написання структурних формул моносахаридів найчастіше використовуються проекційні формули, запропоновані У. Хеуорсом. Слід пам'ятати, що при написанні структурних формул, за Хеуорсу, гідроксильна група при С, буде розташована нижче площини кільця в а- формі і вище в [3-формі:
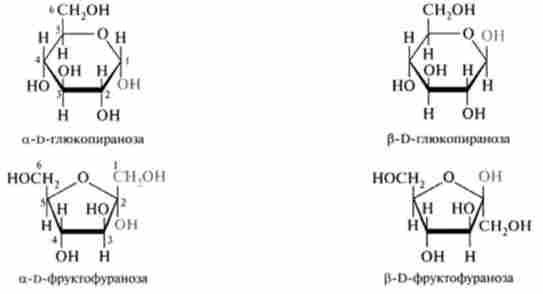
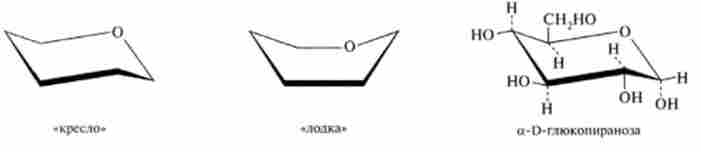
Однак ці формули не відображають просторового розташування атомів в молекулі цукрів. У природі пиранозного кільце не є плоским і може виникнути велика кількість конформаций: шість у формі «човна» і дві в формі «крісла». Форма «крісла» є більш стійкою, і, мабуть, вона переважає в більшій частині природних вуглеводів.
Нижче представлені дві ізомерні форми пиранозного кільця, зображені за допомогою конформаційних формул ( «човен» і «крісло»), а також формула a-D-глюкопіраноз, що має конформацію крісла: