| Головна |
| «« | ЗМІСТ | »» |
|---|
Важливою характеристикою розчину є концентрація. Від цієї величини залежать властивості розчинів.
Концентрацією речовини - компонента розчину - називають величину, що вимірюється кількістю розчиненої речовини, що міститься в певній
масі або об'ємі розчину або розчинника.
Найбільш часто вживані способи вираження концентрації: масова частка. молярна, моляльна концентрація еквівалента, молярна частка, об'ємна частка, титр.
Масова частка w (X) виражається в частках одиниці, відсотках (%), проміле (% о, тисячна частина числа) і в мільйонних частках (млн). Масову частку розраховують за формулами
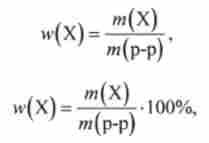
де v (X) - маса даного компонента X (розчиненої речовини), кг (г); т (Р-р) - маса розчину, кг (г).
молярна концентрація с (Х) виражається в моль / м3, моль / дм3, моль / см3, моль / л. моль / мл. У медицині краще застосування одиниці моль / л. Молярна концентрація розраховують за формулою
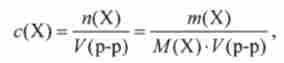
де п (X) - кількість розчиненої речовини системи, моль: М (Х) - молярна маса розчиненої речовини, кг / моль або г / моль; т (Х) - маса розчиненої речовини, відповідно кг або г; V (Р-р) - об'єм розчину.
Моляльна концентрація Ь (Х) виражається в одиницях моль / кг. Форма запису, наприклад: /> (НС1) = 0,1 моль / кг. Розраховують моляльну концентрацію за формулою
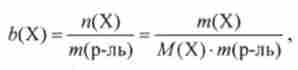
де т (Р-ль) - маса розчинника, кг.
Важливою характеристикою речовини, що розчиняється є розчинність.
Розчинність називають здатність речовини розчинятися в тому чи іншому розчиннику. Чисельно розчинність речовини дорівнює концентрації його насиченого розчину.
Розчинність може бути виражена в тих же одиницях, що і концентрація, наприклад через кількість розчиненої речовини, що міститься в 1 л насиченого розчину (моль / л) або через масу (г) розчиненої речовини в 100 г насиченого розчину. Досить часто розчинність виражають через масу розчиненої речовини (г), що насичує 100 г розчинника. Відповідну величину називають коефіцієнтом розчинності.
Розчинність залежить від природи речовини, що розчиняється і розчинника, температури, тиску, присутності в розчині інших речовин.
Речовини з іонним типом зв'язку і речовини, що складаються з полярних молекул, краще розчиняються в полярних розчинниках, таких, як вода, спирти. Ці розчинники характеризуються високою діелектричної проникністю.
Висока розчинність речовин досить часто обумовлена утворенням міжмолекулярних, зокрема водневих, зв'язків. Так, необмежена взаємна розчинність води і спирту пояснюється утворенням водневих зв'язків між молекулами води і спирту.
Біологічна роль розчинності речовин перш за все пов'язана зі здатністю їх проходити через біологічні мембрани. При перенесенні чужорідних для живих організмів сполук - лікарських препаратів і їх метаболітов- за допомогою простої дифузії тільки жиророзчинні неіонізовані молекули легко проходять через мембрани клітин. Внаслідок цього неелектролітів транспортуються відповідно до їх розчинність в ліпідах (головний компонент мембран), а електроліти - відповідно до ступеня їх дисоціації і розчинність в ліпідах недіссоціірованних молекул.