| Головна |
| «« | ЗМІСТ | »» |
|---|
Гіпофіз, або нижній мозковий придаток, являє собою залозу внутрішньої секреції, яка продукує ряд гормонів, які, в свою чергу, надають регулюючу дію на периферичні ендокринні залози і деякі процеси обміну речовин. Гіпофіз лежить в ямці турецького сідла задньої клиноподібної кістки черепа і пов'язаний з подбугровой областю (гіпоталамусом) за допомогою гіпофізарної ніжки. Анатомічно складається з трьох частин: передньої, найбільш великої (аденогіпофіз); вузької середньої (проміжна); задній (нейрогипофиз) (рис. 12.6). В ембріогенезі аденогипофиз виникає шляхом спинного випинання слизової оболонки ротової порожнини (званої кишенею Ратко) і в міру розвитку втрачає з нею зв'язок, наближаючись до задньої долі. Нейрогіпофіз розвивається як випинання дна III шлуночка мозку, т. е. з одного джерела з гіпоталамусом. Гіпоталамус пов'язаний з нейрогіпофізом гіпоталамогіпофі- Зарн трактом, який в основному включає відростки клітин нейросекреторних ядер переднього гіпоталамуса - супраоптічес- кого і паравентрикулярного. Так звана воротная або портальна судинна система складається з бере початок від верхньої гіпофізарної артерії первинного капілярного сплетення, дренирующего серединна піднесення і переходить в воротні вени, що надходять в передню частку, де вони розпадаються на потужну мережу вторинного капілярного сплетення. Завдяки численним контактам терміналі нейросекреторну волокон різних гіпоталамічних ядер з судинами первинної капілярної мережі стає можливим здійснення нейрогумо- ральних впливів на трофние функції аденогіпофіза. У гіпота- Ламо-гіпофізарної системі кров завжди тече у напрямку
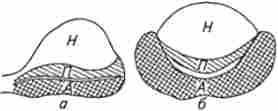
Мал. 12.6. Схема будови гіпофіза:
про - сагиттальний і 0 - фронтальний зрізи; А - аденогипофиз; П - проміжна частка; // - нейрогипофиз від гіпоталамуса до гіпофіза. З синусоидов передньої долі кров витікає через бічні гіпофізарні вени в кавернозні синуси. Проміжна частка гіпофіза порівняно бідна кровоносними судинами, а кровопостачання задньої долі гіпофіза не пов'язане з кровопостачанням передньої долі, вона отримує кров від нижніх гіпофізарних артерій і віддає її через численні вени в кавернозні синуси. Симпатичні нервові волокна до гіпофізу підходять з верхнього шийного ганглія, супроводжуючи кровоносні судини. Решта нервові волокна в гіпофіз йдуть з гіпоталамуса в складі гіпоталамо-гіпофізарного тракту, причому більшість його волокон закінчується в задній частині, але частина проникає в проміжну і передню частки.
Для кожної частки гіпофіза характерна своя структурна організація, що забезпечує виконання специфічної функції в системі координації ендокринних регуляторних впливів.
Аденогіпофіз. За своєю цитоархітектоніка являє собою складну залозу, утворену тяжами епітеліальних клітин (аденоціти), розділених розвиненою мережею синусоїдногокапілярів. За даними светомікроскопічного, цитохимичного і електронно-мікроскопічного досліджень визначено структурні і функціональні особливості різних аденоціти. Виявлено шість різновидів клітин, відповідальних за синтез певного тропного гормону (рис. 12.7).
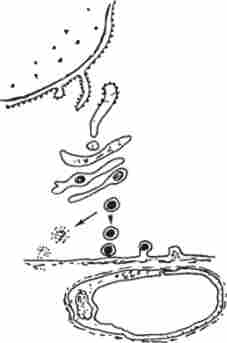
Мал. 12.7. Схема секреторного процесу в аденоціте
Соматотропоціти- ацидофільні клітини, що продукують соматотропний гормон (СТГ) - гормон росту. СТГ регулює синтез нуклеїнових кислот і білка, накопичення білка, мобілізацію жиру з депо і його витрата, накопичення в організмі кальцію, фосфору і натрію, зростання кісток і хрящів, розвиток внутрішніх органів і молокоутворення. Соматотропоціти розташовуються по всьому АДЕНОГІПОФІЗА, переважно в латеральних областях залози. Локалізовані поблизу кровоносних капілярів і вздовж сполучнотканинних септ соматотропоціти представляють собою округлі невеликі клітини з центрально розташованим ядром і виразною грануляцією цитоплазми; деякі клітини можуть мати довгі цитоплазматичні відростки, що досягають перікапіллярним простору. Головною відмінною рисою з- матотропоцітов є наявність в їх цитоплазмі великих секреторних гранул діаметром 350 ... 400 нм. Гранули мають сферичну форму і рівномірну високу електронну щільність.
Функціональна активність соматотропоціти проявляється в числі секреторних гранул. При багаторазовому введенні гормону росту і те, що відбувається за принципом негативного зворотного зв'язку придушенні діяльності залози число секреторних гранул, їх розміри і розміри самої клітини помітно зменшуються, а шорсткий ендоплазматичнийретикулум і комплекс Гольджі (структурні компоненти клітини, відповідальні за синтез і оформлення секреторного продукту) редукуються, т. е. пригнічується синтез і виведення СТГ в кровоносне русло. Навпаки, при введенні гіпоталамічних екстрактів, що містять фактор, що стимулює віддачу СТГ з гіпофіза, в соматотропоціти спостерігається посилене виведення секреторних гранул в перікапіл- лярная простір, а також гіпертрофія шорсткого ЕПР і комплексу Гольджі. Незважаючи на інтенсивне виведення секреторних гранул, їх число в клітці не відрізняється від норми, що говорить про стимуляцію не тільки виведення, а й синтезу СТГ.
Діяльність соматотропоціти знаходиться під контролем гіпоталамічних структур. При розвитку ожиріння, викликаного електролітичним руйнуванням вентромедіальних ядер гіпоталамуса, виявляється помітне накопичення секреторних гранул і поява лізосом, здатних руйнувати невикористані секреторні гранули. При руйнуванні дорсомедіальних ядер в соматотропоціти спостерігається зменшення числа секреторних гранул. Таким чином, гальмування виведення секреторних гранул зумовлено гальмуванням секреції соматолиберина (GRF) після руйнування вентромедіальних ядер, а посилення виведення секреторного продукту з соматотропоціти при руйнуванні дорсомедіальних ядер пов'язано зі зниженням активності фактора, гальмуючого виведення гормону росту (соматостатину, GIF).
Лактотропоціти - другий тип ацидофільних клітин, що продукують лактотропного гормон (ЛТГ), або пролактин, які відрізняються від соматотропоціти більшими розмірами і неправильною формою. У цитоплазмі лактотропоцітов містяться нечисленні секреторні гранули діаметром 600 ... 800 нм, що відрізняються високою електронною щільністю і подовженою формою. Лактотропоціти рідко зустрічаються у статевозрілих самців і самок до досягнення ними статевої зрілості. Число цих клітин значно зростає в аденогипофизе до кінця вагітності і в період лактації. У лактаційний період лактотропоціти містять високорозвинений шорсткий ендоплазматичнийретикулум, безліч пов'язаних рибосом і розширений комплекс Гольджі з численними незрілими секреторними гранулами. Зрілі гранули лежать по периферії клітин поблизу плазматичної мембрани.
Після припинення лактації число активних лактотропоці- тов знижується, а число структурних компонентів клітини, відповідальних за здійснення секреції, істотно зменшується. Різке переривання лактаційного процесу - відбирання шмаркачів через 12 ... 18 год - призводить до накопичення в цитоплазмі зрілих секреторних гранул, а через 24 год в цитоплазмі з'являються лізо- соми, які поглинають і перетравлюють «непотрібні» продукти секреції. Якщо в цей період самкам повернути потомство, то вже через 5 ... 15 хв виведення секреторних гранул посилюється і їх число в цитоплазмі значно зменшується. Відповідно до цих ультраструктурнимі перебудовами змінюється і рівень пролактину в плазмі крові: припинення годування знижує рівень пролактину, а його відновлення підвищує.
Тіреотропоціти-ацидофільні клітини, що продукують тиреотропний гормон (ТТГ) - тиреотропин, який стимулює функції щитовидної залози, сприяє накопиченню в ній йоду і утворення гормонів (трийодтироніну і тироксину). ТТГ посилює розпад тиреоглобуліну і сприяє переходу активної форми гормону в кров. Тіреотропоціти - це полігональні або отростчатие базофільні клітини, розташовані переважно в центральній зоні аденогипофиза, їх число порівняно невелика і складає 1,8 ... 2,9% загального числа секреторних клітин цієї частки. Цитоплазма тіреотропоцітов містить дрібні секреторні гранули діаметром 80 ... 150 нм; найбільші секреторні гранули ТТГ виявлені в аденогипофизе великої рогатої худоби (300 ... 400 нм). Структурні компоненти, які беруть участь в секреторному процесі в тіреотропоцітах, розвинені порівняно мало. Шорсткий ендоплазматичнийретикулум представлений невеликими бульбашками і короткими канальцами, розподіленими рівномірно по всьому простору цитоплазми. Комплекс Гольджі займає околоядерное положення і представлений невеликими вакуолями і мікробульбашками. Найбільш значні ультра- структурні зміни спостерігаються в тіреотропоцітах при виключенні функції щитовидної залози (оперативним шляхом або введенням тиреостатичних препаратів), т. Е. При дефіциті тиреоїдних гормонів. У перші дні після видалення щитовидної залози число тіреотропоцітов в аденогипофизе швидко збільшується, а при поглибленні гіпотиреоїдного стану ці клітини трансформуються в клітини тіреоідекгоміі. В розширених вакуолях цих клітин відзначається накопичення великих електронно-щільних гранул, особливого розвитку досягає комплекс Гольджі, і в міру збільшення терміну після операції він прогресивно розширюється. В подальшому в цитоплазмі з'являються лізосоми, що контактують зі структурами комплексу Гольджі і елімінує зайві секреторні гранули. Тиреоїдні гормони, введені нормальним або тіреоідектомірованним тваринам, гальмують виділення ри- лізинг-факторів тиреотропного гормону (TRF), в результаті чого в аденогипофизе підвищується вміст ТТГ. Додаткове введення таким тваринам TRF стимулює посилення інтенсивності виведення секреторних гранул з клітин. При багаторазовому введенні TRF кількість тіреотропоцітов в аденогипофизе збільшується, а в клітинах наявні морфологічні ознаки інтенсифікації секреторного процесу.
Кортикотропоцити відповідальні за синтез корті- котропіна, або адренокортикотропного гормону (АКТГ), який викликає зростання пучкової і сітчастої зон кори надниркових залоз і стимулює глюкокортикоидную функцію. За даними іммуноцітохіміі з продукцією АКТГ пов'язують хромофобние (які не сприймають барвники) аденоціти, що мають неправильну або зірчасті форму. У цитоплазмі Кортикотропоцити розташовуються нечисленні секреторні гранули діаметром 200 ... 260 нм, локалізовані уздовж плазматичних мембран. Посилення адрено- кортикотропного функції аденогіпофіза морфологічно виражається в глибокій дегрануляции Кортикотропоцити і гіпертрофії шорсткого ЕПР і комплексу Гольджі, що спостерігається при адреналектоміі або введенні препаратів, що пригнічують синтез кортикостероїдів.
Гонадотропоціти. У гіпофізі тварин виробляється два гонадотропних гормону - фолікулостимулюючий (ФСГ) і лютеїнізуючого (Л Г), які доповнюють один одного в своєму фізіологічну дію на статеві залози. ФСГ, або фоллітропін, у самок регулює розвиток і дозрівання фолікулів в яєчниках, у самців - сперматогенез. ЛГ, або лютропін, у самок при спільній дії з ФСГ забезпечує овуляцію і утворення жовтого тіла в яєчниках, у самців стимулює розвиток інтерстиціальної тканини в сім'яниках і вироблення чоловічого статевого гормону тестостерону.
ФСГ-гонадотропоціти - це великі округлі базофільні клітини, розташовані поблизу капілярів по периферії аденогипофиза. Відмінною рисою ФСГ-гонадогропоцітов служить наявність в їх цитоплазмі численних секреторних гранул діаметром 200 ... 300 нм, які зазвичай розташовані рівномірно у всій цитоплазмі клітин. Гранули оточені чітко вираженою мембраною, яка або щільно прилягає до її вмісту, або відокремлена від нього вузьким світлим обідком. Часто на місці розпаду секреторних гранул безпосередньо в цитоплазмі клітин залишаються дрібногранулярна залишки середньої електронної щільності.
Ендоплазматичнийретикулум в ФСГ-гонадотропоціти представлений невеликими вакуолями або сплощеними канальцами, розташованими зазвичай по периферії клітин. Ступінь розвитку ЕПР значно варіює залежно від функціонального стану клітини. Комплекс Гольджі особливо добре розвинений і має кільцеподібної форми, причому внутрішня зона кільця утворена сплощеними ламелами, а наго ружной - дрібними і великими вакуолями. Усередині кільця знаходяться численні мікропухирці (гладкі і облямовані) і секреторні гранули на різних стадіях дозрівання.
Лютеїнізуючого гонадотропоціти (ЛГ-гонадотропоціти) відносяться до групи базофільних клітин, але при цьому здатні виявляти деяку ацидофілія, що дозволяє відрізняти їх від ФСГ-гонадотропоціти, забарвлюються тільки основними барвниками. Л Г-гонадотропоціти розташовуються поблизу долі гіпофіза, а також в центрі залози, причому ці клітини відрізняються від ФСГ-гонадотропоціти подовженою або полігональної формою і секреторними гранулами, діаметр яких досягає 250 нм. На відміну від ФСГ-гонадотропоціти в цитоплазмі Л Г-гонадотропоціти розмір секреторних гранул НЕ варіює і відсутні набухають гранули низькою електронної щільності. Ендоплазматичнийретикулум розвинений слабо і представлений тонкими канальцями, що несуть на своїй поверхні рибосоми. Комплекс Гольджі компактний. Якщо у самців ФСГ-гонадотропоціти зазвичай містять велику кількість секреторних гранул, то у самок наявність секреторного продукту в цитоплазмі залежить від стадії естрального циклу. У діеструса клітини містять невелику кількість секреторних гранул, на початку проеструса розміри клітин збільшуються і вони заповнюються гранулами, при еструс відбувається інтенсивна дегрануляция клітин, що триває в мет- еструс. У діеструса знову зменшуються розміри клітин і відзначається незначний вміст секреторних гранул.
ЛГ-гонадотропоціти рідко виявляють в аденогипофизе самців, а у самок ці клітини представлені більш значно і зміст секреторного продукту відповідає фазам естрального циклу. У діеструса зміст гранул секрету незначно, в проеструса відзначається зростання секреторної активності, яка знижується в стадії еструс. У метеструса гранули знову з'являються, але в діеструса їх кількість знову зменшується. В умовах постійного еструса, що досягається введенням естрогенів, секреція ФСГ залишається незмінною, в той час як секреція Л Г істотно пригнічується. Секреція ФСГ пригнічується при постійному діеструса, ФСГ-гонадотропоціти містять рідкісні секреторні гранули, в той час як ЛГ-гонадотропоціти виглядають активованими. У кастрованих тварин в гонадотропних клітинах гіпофіза відбуваються найбільш глибокі ультраструктурні зміни: в ФСГ-гонадотропоціти відзначається розширення вакуолей ЕПР і зникнення великих секреторних гранул, далі йде інтенсивна вакуолізація, гіпертрофія комплексу Гольджі і прогресивна дегрануляция клітин. Надалі розширені порожнини ЕПР зливаються, заповнюються коллоідоподобним речовиною, у вузькому обідку цитоплазми виявляються лізосомоподобние тільця - клітини набувають вигляду, характерного для клітин кастрації. ЛГ-гонадотро- поііти реагують на кастрацію значно слабкіше: число секреторних гранул кілька збільшується аж до 14сут після операції і лише потім поступово зменшується.
Ліпотропоціти продукують недавно виявлений гормон гіпофіза - ліпотропін. Відомі дві форми цього гормону: альфа- і бета-липотропини, що мають потужний жиромобилизующего дією. У гіпоталамусі і гіпофізі липотропини служать попередниками енкефалінів і ендорфінів, що володіють морфіноподібних дією. Іммуноцітохімічес- кими методами виявлено розподіл ліпотропоцітов: або групове, або в стінці фоллікулоподобних структур аденогіпофіза. Ультраструктурная організація цих клітин відрізняється високим ступенем розвитку структурних компонентів клітин, які здійснюють секреторний процес: щільний цитоплазматичний матрикс, велика кількість органел і секреторних гранул діаметром 250 ... 500 нм. Методами іммуноцітохіміі виявляються і інші більш дрібні і менш диференційовані клітини, які вважають структурами, що знаходяться на більш ранніх етапах диференціювання.
Розроблено тонкі прийоми хірургічного видалення гіпофіза у тварин, які після гіпофізектоміі можуть жити досить довго. Не будучи життєво важливим органом, гіпофіз все ж має суттєвий вплив на стан організму, особливо молодих тварин. Після видалення гіпофіза 2-місячні цуценята дуже відстають у рості, вкрай мляві і малорухливі, основний обмін у них знижений на 20 ... 50%, а температура тіла нижче нормальної на 1 ... 1,5 ° С; спостерігається ожиріння, статеві залози не розвиваються, а статеві інстинкти не виявляються; розміри щитовидної залози і кори надниркових залоз залишаються значно меншими за звичайні, а тимус не береться інволюції. У дорослих тварин видалення гіпофіза призводить до зниження рівня енергетичного обміну, зміни обміну білків, жирів і вуглеводів; розміри щитовидної залози, кори надниркових і статевих залоз зменшуються, а в яєчниках припиняється дозрівання фолікулів, овуляція і утворення жовтих тіл. Трансплантація тканини гіпофіза або введення її екстрактів запобігають розвитку дегенеративних процесів, зазвичай наступаючих у тварин при гіпофізектоміі. Тривале введення екстрактів речовини гіпофіза інтактним молодим тваринам викликає у них надмірний ріст, у тварин більш старшого віку проявляється акромегалія (посилений ріст трубчастих кісток) і поява певних пухлин.
Середня (проміжна) доля - вузька пластинка багатошарового епітелію, відокремлена від передньої долі гіпофізарної щілиною, а від нейрогипофиза прошарком сполучної тканини, яка містить кровоносні судини і базальну мембрану. Проміжна частка гіпофіза утворює меланоцітстімуліруюшій гормон (МСГ), званий також інтермедін або меданотропіном. Відомі дві форми: альфа- і бета-МСГ, що представляють собою поліпептиди, які в організмі забезпечують пігментний обмін шкіри, волосся, райдужної і сітчастої оболонок ока. Мелано- трофний гормон бере участь також в процесах адаптації зорового аналізатора.
З боку гіпофізарної щілини проміжна частка гіпофіза покрита шаром сплощені маргінальних клітин. Лю менальная (звернена в просвіт гіпофізарної щілини) плазматична мембрана містить короткі мікроворсинки і вії, а сусідні маргінальні клітини скріплені сполучними комплексами. За шаром маргінальних клітин знаходиться паренхіма проміжної частки, утворена декількома рядами залізистих клітин; переважають клітини, що виробляють МСГ. Меланотропоціти мають полігональну форму і з'єднуються між собою десмосомами. Відмінною характеристикою меланотропоцітов служить наявність в їх цитоплазмі великої кількості секреторних гранул діаметром 200 ... 500 нм. Другий різновидом залізистих клітин проміжної частки гіпофіза є зірчасті клітини - це рідко зустрічаються невеликі клітини, локалізовані між великими мелано- тропоцітамі і простягається між ними довгі цитоплазматичні відростки. Відростки цих клітин з'єднуються між собою за допомогою десмосом. Кілька об'єдналися зірчастих клітин здатні формувати псевдофоллікуліт, порожнину якого заповнюється колоїдним вмістом. Об'єднані між собою клітини утворюють потужні сполучні комплекси, а на поверхні клітин, зверненої в просвіт фолікула, сформовані микроворсинки і вії. У паренхімі проміжної частки гіпофіза присутні також клітини, схожі за ультраструктурной організації з Кортикотропоцити аденогипофиза, але вони містять менші за розмірами гранули (менше 200 нм). Ці клітини поблизу від нейрогипофиза утворюють значні скупчення в ростральної частини, де проміжна частка переходить в аденогіпофіз. При електронно-мікроскопічному дослідженні в проміжній частці виявлено нервові волокна і їх термінали, що утворюють сінаптоідние контакти з залозистими клітинами. Описано три види закінчень: холинергичні, адренергічні і пептідергічні. Найбільш часто такі контакти присутні на поверхні меланотропоцітов і кортікотропоцітоподобних клітин.
Функціональна активність клітин проміжної частки гіпофіза в значній мірі залежить від рівня в крові гормонів кори надниркової залози. Після адреналектоміі ширина цієї частки помітно збільшується за рахунок гіпертрофії залізистих клітин. В ме ланоцітах відбувається глибока дегрануляция, гіпертрофія комплексу Гольджі і ЕПР. При введенні тваринам кортикостероїдних гормонів ширина проміжної частки, навпаки, зменшується і клітини стають більш компактними. Існує досить багато підстав до того, щоб вважати можливим виділення АКТГ і МСГ залозистими клітинами проміжної частки і що це пов'язано з послідовністю синтезу гормонів: спочатку синтезується АКТГ, є прогормоном для альфа-МСГ. Функції МСГ у ссавців не обмежуються тільки процесами меланогенеза. Поряд з іншими гормонами фізіологічно активні речовини проміжної частки здатні брати участь в реакціях адаптації організму до нейрогенному і осмотичного стресу.
Нейрогіпофіз - задня частка гіпофіза. Самостійна залоза внутрішньої секреції. Нейрогемальний орган, в якому накопичуються і з якого виводяться в кровоносне русло нейрогормони - вазопресин і окситоцин, віднайдені в крупноклітинних ядрах гіпоталамуса. Нейросекреторні клітини супраоптічес- кого і паравентрикулярного ядер гіпоталамуса поряд із загальними рисами будови типових нейронів мають і деякими характерними особливостями. Діаметр аксона у місця відходження від тіла клітини дуже великий, що, очевидно, пов'язано з інтенсивним аксональним транспортом нейросекрета. Основними структурними компонентами нейрогипофиза служать нейросекреторні аксони, іхтерміналі, що закінчуються на капілярах, і особливі гліальні клітини - пітуіціти. Нейросекреторні волокна діаметром від 400 до 600 нм йдуть зазвичай паралельно один одному і зібрані в невеликі групи. Розширення і термінали волокон містять нейросекреторні гранули (150 ... 200 нм), мікротрубочки і нейропротофіламенти. Закінчення нейросекреторну волокон межують з перікапіллярним простором, утворюючи аксоновазальние контакти. Паренхіма нейрогипофиза пронизана численними капілярами, ендотеліальні клітини яких сильно сплощені і містять велику кількість фе вільн діаметром близько 500 нм, перекритих тонкими діафрагмами. За розмірами і ультраструктурі пітуіцітов ці клітини поділяються на кілька типів за аналогією з гліальними клітинами центральної нервової системи: розрізняють астро-, оліго- і мікропітуіціти.
Астропітуіціти - найбільші клітини, що мають довгі цитоплазматичні відростки, багато з яких закінчуються поблизу перікапіллярним простору і стелить на деякому протязі базальнумембрану капілярів.
Олігопітуіціти - найчастіші клітини, на відміну від астропітуіцітов мають меншу кількість відростків, в них більш розвинений шорсткий ендоплазматичнийретикулум. Характерна їх особливість - наявність в цитоплазмі численних ліпідних крапель.
Мікропітуіціти зустрічаються відносно рідко, мають невеликі розміри і дуже щільне ядро неправильної форми, але відростків у них трохи або вони зовсім відсутні. Цитоплазматичні відростки декількох пітуіцітов можуть з'єднуватися один з одним за допомогою десмосом, формуючи своєрідну мережу, в петлях якої знаходяться групи нейросекреторну волокон і їх варикозні розширення (тільця Герінга).
Нейрогормони задньої долі гіпофіза безпосередньо беруть участь в регуляції водносолевого обміну, і будь-які зрушення водносолевого рівноваги відображаються в тій чи іншій мірі на ультраструктурі органу. В умовах сольовий навантаження швидко зменшується число нейросекреторну гранул, з'являються залишкові гранули і безліч мікропухирців. Аналогічні ознаки активації виведення нейросекрета виявляються у тварин з спадковим і експериментальним (аллоксановим) діабет і після адреналектоміі. У цих випадках в більшості нейросекреторну волокон відсутні нейросекреторні гранули, і вони заповнені великою кількістю мікропухирців. Пригнічення функціональної активності гіпоталамо-нейрогіпофізар- ної системи і блокування виведення нейрогормонов в кров наступають при гіпергідратації або введенні альдостерону. При цьому в нейрогіпофіз відзначається масивне накопичення нейросекреторних гранул в волокнах, їх розширеннях і великих тільцях Герінга, а також зменшення числа нейротрубочек і мікропухирців. Надлишок накопичених нейросекреторну гранул може віддалятися за допомогою лізосомальних апарату.
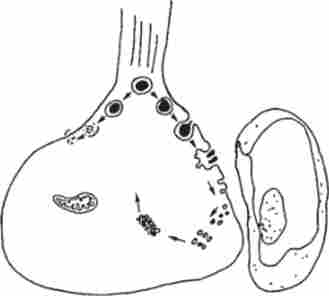
Мал. 12.8. Схема виведення секреторного матеріалу в терміналах нейрогипофиза
Існують переконливі докази виведення вмісту нейросекреторних гранул з терминалей нейросекреторну аксонів шляхом екзоцитозу. Мембрана нейросекреторної гранули зливається з мембраною Нейросекреторні закінчення, на місці злиття утворюється отвір, через яке вміст гранули переходить в перікапіллярним простір. В результаті інтенсивного включення мембрани гранул до складу плазматичної мембрани Нейросекреторні закінчення може накопичитися надлишок мембранного матеріалу, який видаляється за рахунок спеціального механізму утворення мікробульбашок в результаті ендоцитозу плазматичноїмембрани нейросекреторну закінчень. Мікропухирці відходять від аксолемми і формують скупчення правильної гексагональної форми (рис. 12.8). В умовах, коли виділення нейросекреторну гранул НЕ інтенсифікується, нейросекрет виділяється у вигляді молекулярних комплексів через неушкоджену мембрану нейросекреторної гранули і плазматичну мембрану нервового закінчення. При різкому збільшенні виведення нейрогормонов переважаючим стає механізм екзоцитозу. В цьому випадку активується діяльність нейротрубочек і нейропротофіламентов, які забезпечують переміщення нейросекрета і облітають контакт гранул з аксолеммой.
Продукти секреторною діяльності паравентрикулярного і супраоптичного ядер гіпоталамуса, що виділяються в кров із задньої долі гіпофіза, являють собою октапептід циклічної природи: окситоцин і вазопресин, або антідіуретічес- кий гормон (АДГ). Окситоцин викликає скорочення гладкої мускулатури матки і міоепітелія молочної залози. У самок під час пологів окситоцин викликає і стимулює перейми і вигнання плоду.
Ступінь чутливості матки до оксітоііну залежить від виду тварини і його фізіологічного стану. Естрогени (жіночі статеві гормони) підвищують реакцію матки, особливо висока вона в середині статевого циклу в період овуляції, відповідний фазі тічки. Виділення окситоцину в кров під час спарювання збільшує частоту і амплітуду скорочень матки, що забезпечує переміщення сперми по статевих шляхах в яйцепровід. Після овуляції починає функціонувати жовте тіло, продукується прогестерон і чутливість матки до оксітоці- ну істотно знижується. Вкрай низька відповідна реакція матки на окситоцин в початковий період вагітності, але в подальшому чутливість підвищується, досягаючи максимуму безпосередньо перед пологами.
Викликане окситоцином скорочення міоепітелія сприяє видаленню молока з порожнини альвеол молочної залози, підвищує цистернальних і внутрипротоковое тиск, активуючи молокоотдачу. У самців окситоцин, очевидно, збільшує скорочення спермопроводящіх шляхів, забезпечуючи процес еякуляції. У крові окситоцин швидко руйнується специфічним ферментом оксітоціназа. Активність цього ферменту досить висока у вагітних самок і під час пологів, але різко знижується в перші дні після пологів.
АДГ відповідальний за стимуляцію реабсорбції води з первинної сечі в дистальному відділі ниркових канальців, а також впливає на мінеральний обмін, гальмуючи реабсорбцію калію, натрію і хлоридів. Разом з цим АДГ викликає скорочення артеріол і капілярів, діючи безпосередньо на клітини гладеньких м'язів, що веде до загального підвищення артеріального тиску. Слід, однак, зауважити, що для підвищення кров'яного тиску необхідні дуже великі дози гормону, що значно перевищують дози, які надають антидиуретичний ефект. Дія вазопресину на чутливі тканини досить короткочасно: через 1 ... 3 хв активність введеного гормону знижується вдвічі за рахунок руйнування в печінці та нирках, а 8 ... 10% його виділяється з сечею.
Інтенсивно розвивається розділ фізіології, що вивчає взаємодію гормонів та інших біологічно активних речовин з рецепторами, розташованими в ЦНС, являє гіпоталамо-гіпофізарну систему в абсолютно новому аспекті. Пептидні гормони утворюють якісно новий клас ендогенних регуляторів функцій нервової системи і організму в цілому. Деякі з них (наприклад, вазопресин, окситоцин, кортико- тропин, тіроліберін) були відомі і раніше, але в якості гормонально-активних субстанцій з певними, узкоспеціфічнимі функціями. Новизна цього класу речовин обумовлена походженням ряду сполук з одного попередника - пропіомеланокортіна, з якого утворюються пептиди, що діють подібно морфіну і здатні впливати на багато функцій органів і систем організму. Увага, сприйняття болю, харчове і статеву поведінку, забезпечення гомеостазу при стресових впливах, адаптації організму до екстремальних умов - це все прояви негормональних функцій за рахунок здійснення зв'язку між нейронами, передача міжнейронної інформації, модуляція функціонального стану нейронів. Клітини, які продукують пептиди, і клітини, чутливі до них, утворюють потужну гипоталамичну пептідергічної мережу, що охоплює головний і спинний мозок. Вплив ендогенних пептидів на ендокринну систему дозволяє їм інтегрувати безліч поведінкових реакцій, що говорить про тісний функціонального взаємозв'язку між медіаторнимі і ендокринними системами. Так, вазопресин і його синтетичні аналоги впливають на закріплення умовних рефлексів, окситоцин бере участь в оптимізації статевої поведінки, а меланостатин і тіроліберін мають антидепресивними властивостями.
Спільність певних ділянок молекули АКТГ з ендорфі- нами і бета-ліпотропін, обумовлена походженням з одного попередника, пояснює вплив кортикотропіну на багато функцій організму: придушення агресивності, благотворний вплив в стресових ситуаціях, надання транквілізуючі ефекту. Ендорфіни мають виражену опіоїдної (морфіноподібними) активністю, і їх застосування досить перспективно при необхідності досягнення анальгетичного ефекту. Використання таких речовин для фармакологічної корекції патологічних станів організму можливо, так як виявлені терапевтичні властивості пептидів як природних регуляторів фізіологічних і біохімічних процесів. Значні перспективи має і те, що ці речовини ефективні в дуже низьких концентраціях, не накопичуються в організмі і нетоксичні.