| Головна |
| «« | ЗМІСТ | »» |
|---|
Найбільш важливі фосфогліцерідов є компонентами мембран, а також ліпопротеїдів, що виконують транспортну функцію. Ці фосфогліцерідов утворюються по розгалуженому метаболічного шляху, що починається з фосфатидного кислоти

Реакції шляхів біосинтезу фосфогліцерідов (рис. 9.18) локалізовані головним чином в ендоплазматичної мережі. Спочатку фосфатидними кислота в результаті оборотної реакції з СТР перетворюється в цітіділдіфосфатдіацілгліцерін, який служить загальним попередником всіх фосфогліцерідов, що утворюються цим шляхом.
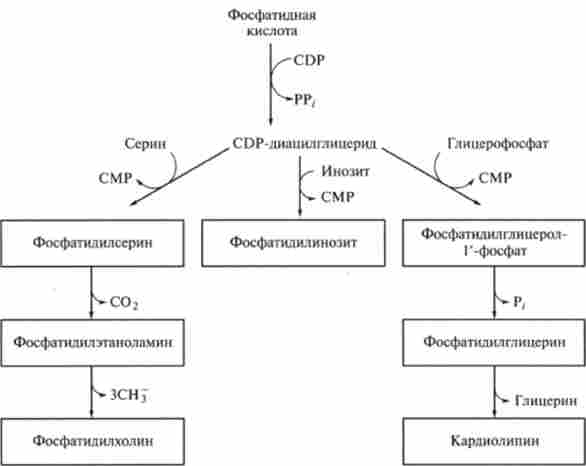
Мал. 9.18. Метаболічні шляхи біосинтезу фосфогліцсрідов
Цітіділдіфосфатная частина СDP-діацілгліцеріда може розглядатися як переносник фосфатидного кислоти. У наступних реакціях, кожна з яких каталізується специфічним ферментом, цітіділмонофосфат витісняється з молекули CDP-діацілгліцеріда одним з трьох спиртів: гліцерофосфатом, серином або інозитом - з утворенням З-фосфатіділгліцерол-Г-фосфату. фосфаті- ділсеріна або фосфатіділінозіта відповідно.
Ферментативне декарбоксилирование залишку серину в молекулі фосфаті- ділсеріна призводить до утворення фосфатидилетаноламін, який служить попередником фосфатидилхоліну, що утворюється в результаті послідовного перенесення трьох метильних груп від трьох молекул донора метильних груп S-аденозілметіонін до аміногрупи залишку етаноламіну.
Продуктами цих трьох послідовних реакцій метилювання є фосфатіділмонометілетаноламін. фосфатіділдіметілетаноламін і фосфаті- ділхолін. Освіта фосфатидилхолина з фосфатіділдіметілетаноламіна описується рівнянням
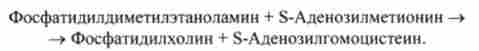
Спочатку етаноламін за участю відповідної кінази фосфорілі- руется з утворенням фосфоетаноламіна. Потім фосфоетаноламін взаємодіє з СТР, в результаті чого утворюються цітіділдіфосфатетаноламін (CDP- етаноламін) і пірофосфат (РР,). У наступній реакції З DP-етанол амін, взаємодіючи з 1,2-дигліцеридів, що утворюється при дефосфорилюванні фосфатидного кислоти, перетворюється в фосфатіділетаноламін. Реакція, що каталізується ферментом етаноламінфосфотрансферазой, записується таким чином:
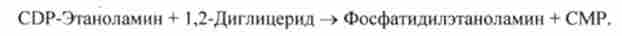
Як показано вище, фосфатидилхолін (лецитин) може синтезуватися в результаті послідовного перенесення трьох метильних груп від трьох молекул S-аденозил метіоніну до аміногрупи залишку етаноламіну.
Існує ще один шлях синтезу фосфатидилхоліну в клітинах тварин. У цьому випадку, як і при синтезі фосфатидилетаноламін, використовується СТР як переносник, але вже не фосфоетаноламіна, а фосфохоліна. На першому етапі синтезу вільний холін активується під дією холінкінази з утворенням фосфохоліна:
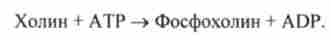
Потім фосфохолін реагує з СТР, утворюючи цітідіндіфосфатхолін (CDP- холін):
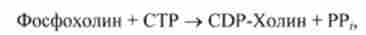
після чого CDP-холін взаємодіє з 1,2-дигліцеридів і в результаті виходить фосфатидилхолин:
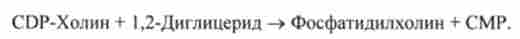
Фосфатидилсерин у ссавців синтезується в реакції обміну етаноламіну на серин наступним шляхом (за участю іонів Са2+):
Фосфатіділетаноламін + L-Серін -> Фосфатидилсерин + Етаноламін.
Існує і другий шлях освіти фосфатидилсерина, який пов'язаний з попередніми залученням фосфатидного кислоти в синтез фосфогліцерідов. Відбувається перенесення серина на фосфатідільний залишок з утворенням фосфатидилсерина:
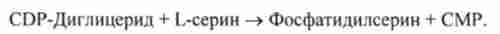
Таким же шляхом виходить фосфатидилинозитол.
Сфінгомієлін синтезується в результаті взаємодії цераміду з CDP- холін. Интермедиатом в біосинтезі сфінгоміеліна є церамід (N-ацил- сфингозин), який утворюється при взаімодствіі сфингозина з ацил-КоА:
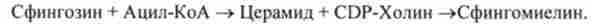
Біосинтез холестерину. Метаболічний шлях ферментативного синтезу холестерину налічує понад 35 ензиматичних реакцій (рис. 9.19). На цьому шляху можна виділити три основні стадії.
1. Перетворення активного ацетату CH3-CO-S-K0A в мевалоновую кислоту (Сб):
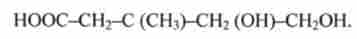
2. Освіта з мевалонової кислоти сквалена (С30):
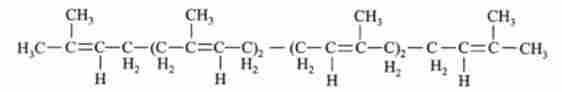
3. Циклизация сквалена в холестерин - тетрациклічними липид (НЕ гліцерид):
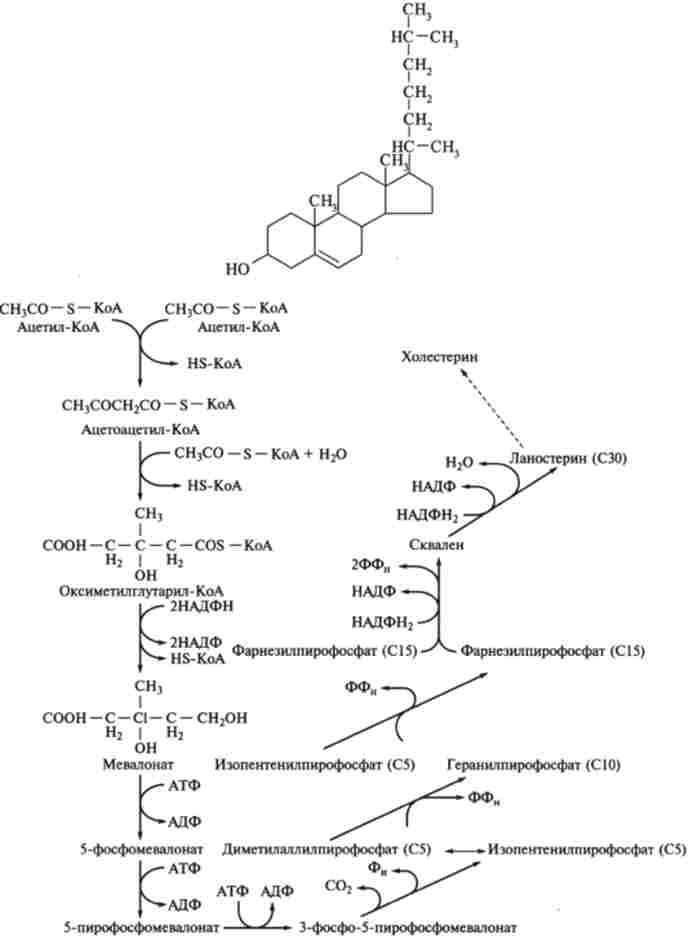 Мал. 9.19. Метаболічний шлях біосинтезу холестерину
Мал. 9.19. Метаболічний шлях біосинтезу холестерину
Фізіологічна роль холестерину описана в розд. 8.4. Холестерин виконує в організмі структурну функцію - входить в якості компонента до складу клітинних мембран - і метаболічну функцію - служить попередником при синтезі стероїдів - жовчних кислот, стероїдних гормонів, вітаміну D3.
В організм дорослої людини з їжею в залежності від її роду вводиться щодня 300-500 мг холестерину частково у вільному вигляді, частково у вигляді ефірів жирних кислот. Ефіри гідролізуються на холестерин і жирні кислоти ферментом панкреатичного соку холестерінестеразой. Активність ферменту проявляється при впливі жовчних кислот.
Джерелом холестерину в тонкій кишці є: їжа (0,3-0,5 г / сут, у вегетаріанців значно менше); жовч (з жовчю в тонку кишку виділяється 1-2 г / сут ендогенного холестерину); слущенний епітелій шлунково-кишкового тракту і кишкові соки (до 0,5 г / добу).
В цілому в кишечник надходить 1,8-2,5 г / сут ендогенного і екзогенного холестерину. З цієї кількості близько 0,5 г / сут холестерину виділяється з фекаліями у вигляді відновленого продукту - капростеріна і невелика частина у вигляді окислених продуктів - холестенонов.
Відновлення і окиснення холестерину відбуваються в товстій кишці під впливом ферментів мікробної флори. Основна частина холестерину в довільній формі піддається всмоктуванню в тонкій кишці в складі змішаних жирових міцел.
Починаючи з сквалена всі проміжні продукти біосинтезу холестерину (як і сам холестерин) нерозчинні у водному середовищі. Тому вони беруть участь в кінцевих реакціях біосинтезу холестерину, будучи пов'язаними зі стерінперено- сящімі білками (СПБ). Це забезпечує їх розчинність в цитоплазмі клітини і протікання відповідних реакцій. Даний факт має важливе значення і для надходження холестерину в клітинні мембрани, окислення в жовчні кислоти, перетворення в стероїдні гормони.
Як зазначалося вище, реакцією, яка регулює швидкість біосинтезу холестерину в цілому, є відновлення гідроксиду метилглутарил-КоА в мевало- нову кислоту, що каталізує ГМГ-КоА-редуктази. Даний фермент відчуває регуляторний вплив ряду факторів. Зокрема, швидкість синтезу редуктази в печінці схильна чітким добовим коливанням: максимум її доводиться на північ, а мінімум - на ранкові години.