| Головна |
| «« | ЗМІСТ | »» |
|---|
плазма крові є її рідку частину, що залишається після видалення формених елементів. В 1 л плазми крові людини міститься 900-910 г води, 65-80 г білка і 20 г низькомолекулярних сполук. Плазма крові тісно пов'язана з тканинної рідиною, і між ними відбувається дуже швидкий обмін водою і невеликими молекулами. Це дозволяє підтримувати сталість середовища, що оточує всі клітини організму, в умовах їх мінливої метаболічної активності. У плазмі і тканинної рідини істотно різниться тільки концентрація білків, оскільки великі білкові молекули не здатні проходити через стінки капілярів.
Білки плазми крові являють собою суміш безлічі різноманітних протеїнів, молекулярні маси яких варіюють від 44 000 до 1300000 дальтон. Найбільше серед них альбуміну (60% від загальної кількості), а-, (3-, у-глобулінів і фібриногену. Білки плазми крові виконують велику кількість різноманітних функцій:
колоїдно-осмотичну (білки здатні афективно утримувати воду, але не можуть проходити через капілярні стінки, що забезпечує підтримку водного балансу між кров'ю і тканинною рідиною).
Небілкові органічні компоненти плазми крові не приймають безпосередньої участі в реалізації її функцій. Вони просто переносяться кров'ю, мало впливаючи на її властивості. Ця група речовин включає поживні речовини (глюкозу, ліпіди, амінокислоти), продукти проміжного обміну (молочну та пировиноградную кислоти), кінцеві продукти обміну (сечовину, креатин, білірубін та ін.) І біологічно активні речовини (вітаміни, гормони та ін.).
Мінеральні компоненти плазми крові складають в сукупності близько 1% від її маси. Вони представлені, головним чином, електролітами, що дають катіони і аніони (Na+, До+, Са2+, Mg2+, Cl ", НРО2, НСО3). До цієї групи належать також мікроелементи (Fe2+, Cu2+, з2+, I ", F), які більш ніж на 90% пов'язані з органічними речовинами і не мають електролітичними властивостями. Мінеральні компоненти плазми створюють осмотичний тиск, реакцію середовища, беруть участь в тромбообра- зовании (Са2+) І впливають практично на всі функції крові.
найважливіші фізико-хімічні характеристики плазми крові це її осмотичний тиск, онкотичний тиск і реакція середовища. Серед різноманітних показників внутрішнього середовища вони займають одне з головних місць, і їх відхилення від оптимального рівня небезпечно для життєдіяльності організму.
осмотичний тиск являє собою силу, завдяки якій вода переміщається через напівпроникні мембрани клітин з області з низькою концентрацією осмотично активних речовин (електролітів, неелектролітів, білків) в область з їх більш високою концентрацією. Осмотичний тиск плазми крові становить в нормі 5440 мм рт. ст. Близько 80% величини осмотичного тиску плазми обумовлено хлоридом натрію (NaCl). Осмотичні тиску крові, лімфи, внутрішньоклітинної і тканинної рідини близькі за величиною і відрізняються відносною сталістю. Посилення метаболічної активності клітин того чи іншого органу супроводжується короткочасним зростанням осмотичного тиску відтікає крові, яке досить швидко повертається до початкового рівня.
онкотичноготиск являє собою частину загального осмотичного тиску крові і створюється білками плазми. Його величина становить 25-30 мм рт. ст. і на 80% визначається альбумінами. Незважаючи на невелику абсолютну величину, онкотичний тиск відіграє важливу роль в утриманні води в судинному руслі, освіті лімфи і тканинної рідини, всмоктування води з кишечника. При хворобах нирок, коли з сечею виводяться білки, і при захворюваннях печінки, коли знижується синтез альбуміну, онкотичноготиск плазми падає. Це призводить до переходу води з судин в тканині і розвитку набряків.
реакція середовища визначається концентрацією в ній іонів водню (Н+). Концентрацію Н * прийнято виражати через показник pH - негативний десятковий логарифм молярної концентрації Н+:
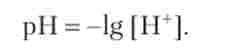
Якщо pH = 7, то концентрація протонів Н+ дорівнює 10 7 моль / л, що відповідає нейтральному розчину чистої води; в кислих розчинах pH < 7; для лужних розчинів характерний pH > 7. pH артеріальної крові становить 7,35-7,45 і є важливим гомеостатичним показником. Зрушення pH крові на 0,1 за вказані межі призводить до порушень в системі дихання; на 0,2 - в системі кровообігу; на 0,3 - в роботі центральної нервової системи. Зрушення pH крові на 0,4, як правило, несумісний з життям.
Основними «мішенями» іонів Н ~ в організмі є ферменти і їх активність, процеси синтезу і розщеплення органічних речовин, а також клітини - рецептори pH. Головним джерелом Н+ в організмі є вугільна кислота Н2С03. Вона утворюється при взаємодії з водою вуглекислого газу, який виробляється клітинами як кінцевий продукт метаболізму поживних речовин. Крім того, в процесі обміну амінокислот і фосфоліпідів в організмі в невеликих кількостях утворюються фосфорна, сірчана, соляна та інші кислоти.
Сталість pH внутрішнього середовища організму підтримується декількома механізмами: буферними системами плазми, роботою легких і роботою нирок.
Буферні системи сформовані слабкими кислотами і сполученими з ними підставами. Вони дозволяють протидіяти зрушень pH при додаванні в невеликих кількостях сильних кислот або лугів. У крові присутні три основні буферні системи: гідрокарбонатна (пов'язана з вугільною кислотою), фосфатна (пов'язана з фосфорною кислотою) і білкова.
Легкі впливають на pH крові, видаляючи надлишок С02 і, відповідно, зменшуючи концентрацію вугільної кислоти - основного джерела Н+.
Нирки впливають на pH крові повільно, але найбільш ефективно. Вони здатні виводити з організму як кислоти, так і підстави, в результаті чого сеча може міняти свій pH в діапазоні від 4,5 до 8.