| Головна |
| «« | ЗМІСТ | »» |
|---|
Пептидні гормони відкриті більш 100 років тому. пептид - це коротка ланцюжок з амінокислот, іншими словами, короткий білок. Чіткої межі між пептидами і білками немає, хоча ланцюжок в 1000 амінокислот завжди називають білком. У 1970-ті рр., Коли в мозку та інших тканинах були виявлені рецептори до рослинного алкалоїду - морфіну, виникло питання, які ж з'єднання є власними лигандами нашого організму до цих рецепторів. Так були виділені перші короткі регуляторні пептиди - енкефаліни. З тих пір в організмах різних видів тварин, а також представників інших царств живих істот (грибів, найпростіших, бактерій) були знайдені багато сотень регуляторних пептидів, об'єднаних в різні класи, підкласи і т. Д.
Найчастіше регуляторні пептиди (РП) впливають на міжклітинні зв'язку в організмі, а внутрішньоклітинна роль їх набагато менше. Пептиди можуть виступати в якості медіатора, комедіатора, нейромодулятора, гормону.
медіатор - речовина, що виділяється з пресинаптичного закінчення і так чи інакше впливає на постсинаптичну клітку, впливаючи на її деполяризацію або гиперполяризацию.
Комедіатор - речовина, що міститься в тілі нейрона і здатне регулювати викид тих чи інших медіаторів, перебуваючи в одних і тих же закінченнях і навіть в одних і тих же везикулах з ними (рис. 10.2).
нейромодулятора - речовини, що викидаються з везикул в синаптичну щілину і, крім зв'язування з постсинаптичними рецепторами, що виходять у міжклітинний простір і що впливають на навколишні нейрони. Серед пептидів нейромодулятора зустрічаються особливо часто.
гормон - речовина, що виділяється з живої клітини без пошкодження її цілісності, що потрапляє в загальний кровотік, що досягає з кровио будь-яких органів і тканин і, якщо на клітинах цих тканин є відповідні рецептори, які надають на них свій вплив.
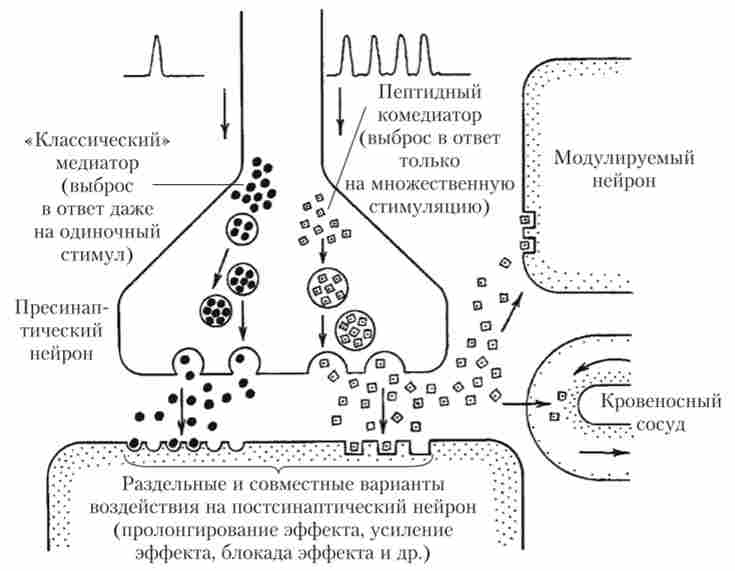
Мал. 10.2. Дія пептидів-регуляторів на синаптичному рівні
Серед пептидів часто зустрічаються регуляторні фактори, які можуть виступати у всіх цих ролях (субстанція Р, вазоактивний інтестинального пептид (ВІП), енкефаліни, соматостатин та ін.), що, звичайно, ускладнює вивчення пептидного системи регуляції.
До пептидним медіаторів не може бути застосована сувора система критеріїв, яким більш-менш відповідають «класичні» медіатори. Пептиди-медіатори синтезуються в цитоплазмі нейронів так званим нерібосомальним шляхом. Мається на увазі, що класичним чином спочатку синтезується (за участю рибосом, мРНК, тРНК) велика молекула білка-попередника, що включає в себе багато послідовностей коротких регуляторних пептидів (рис. 10.3).
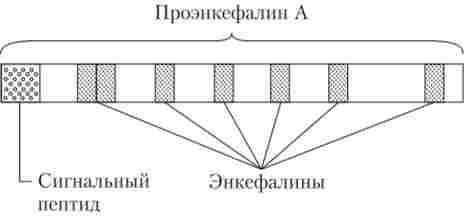
Мал. 10.3. Молекула проенкефалінов А і послідовності енкефалінів в ній
При необхідності ферменти пептідази «відрізають» сигнальний пептид від молекули-попередника, а потім вирізують молекули пептидного медіатора. Дуже важливо, що в один і той же попередник можуть входити послідовності абсолютно різних пептидів з різноманітними функціями, і від набору пептідаз, що містяться в клітці, залежить, які активні пептидні регулятори будуть «виготовлені» з молекули- попередника. Молекули медіатора аксональним транспортом доставляються в нервове закінчення, де концентруються в великих везикулах і викидаються в синаптичну щілину при деполяризації мембрани закінчення і присутності кальцію.
Короткі РП існують в міжклітинному просторі стільки ж, скільки і класичні медіатори, а ось більш великі пептиди набагато стабільніше і можуть надавати тривалий вплив на синаптичну передачу, тим більше що РП зв'язуються зі своїми рецепторами в дуже малих дозах. Таким чином, викинуті в щілину РП можуть шляхом дифузії досягати досить віддалених клітинних структур і надавати на них свою дію.
Пептідергічні нейрони представлені у всіх структурах ГМ, проте з упевненістю говорити про те, що виділяються ними пептиди є медіаторами, - не можна. Більшість цих регуляторних речовин не відповідають критеріям медіаторів і скоріше відносяться до нейрогормонів і нейромодуляторов.
Із застереженнями до медіаторів пептидної природи можна зарахувати: субстанцію Р (SP), ВІП, соматостатин, нейропептид Y (NY), Оніоіди. Практично всі ці пептиди виявлені як в межах НС, так і в інших тканинах. Для всіх цих пептидів характерна полимодальность (множинність) ефектів, і часто важко визначити участь того чи іншого пептиду в фізіологічної реакції саме в якості медіатора, а не, наприклад, нейрогормона.
Всі відомі рецептори до РП є метаботропнимі і пов'язані з G-білками. Найкраще в силу практичних потреб досліджені опіатні рецептори (див. Нижче).
В ході виконання програм по вивченню і розшифровці генома людини були знайдені пов'язані з G-білками рецептори, до яких «не підходить» жоден з відомих ендогенних лігандів. Передбачається, що це рецептори ще не виявлених пептидних медіаторів і комедіаторов.
субстанція Р, або речовина Р (SP) - пептид з 11 амінокислот, у якого були відкриті властивості медіатора. Якщо говорити про ЦНС, то найбільше SP виявлено в чорній субстанції і в задніх рогах СМ, а найменше - в мозочку і гіпокампі. Багато цього пептиду виявлено в периферичної НС. Крім того, SP була знайдена в клітинах нейроглії, що мають відношення до регуляції мозкового кровообігу. SP синтезується в синаптичних закінченнях, а в сомі нейронів, а потім швидким аксони транспортом переміщається в пресинаптичну бляшку, де і концентрується в везикулах. субстанція Р є медіатором первинних сенсорних нейронів спинномозкових гангліїв. Таким чином, нейрони, що містять SP, починають провідні шляхи, але яким в ГМ йде інформація про біль і температурної чутливості. Крім того, цей пептид, мабуть, є медіатором в нігростріальной шляхах. Деполяризуючий ефект виділяється SP на пресинаптичних мембрану набагато сильніше, ніж у глутамату. Виступаючи як модулятор, SP гальмує виділення серотоніну, послаблює аналгетичний ефект опіатів і абстиненцію при скасуванні морфіну у наркоманів. SP часто виявляють в одних синаптичних закінченнях з катехоламинами, серотоніном, АХ, ГАМК, а також іншими РП (вазоактивний інтестинального пептид, соматостатин, опіоїди).
Вазоактивний інтестинального пептид (ВІП), що складається з 28 амінокислот, знайдений у багатьох структурах НС, зокрема в корі великих півкуль і в клітинах гангліїв У НС, де він виконує роль медіатора постгангліонарних нейронів, забезпечуючи розслаблення гладкої мускулатури кровоносних судин, кишечника, бронхів. У парасимпатичних постгангліонарних волокнах ВІП дуже часто супроводжує АХ, хоча в закінченнях ці два комедіатора локалізовані в різних везикулах. Про медиаторной ролі ВІП в ЦНС відомо мало.
соматостатін являє собою пептид з 14 амінокислот, який виробляється в нейронах гіпоталамуса, гальмує вироблення гормонів переднього гіпофіза - гормону росту (соматотропний гормон), тірео- тропного і адренокортикотропного гормонів. Крім своєї дії на ендокринну систему, цей пептид є медіатором у вегетативних і спинномозкових гангліях, гіпоталамусі, миндалевидном комплексі, корі великих півкуль. Соматостатін часто є комедіатором пептидних і непептидним медіаторів, причому, мабуть, частіше він гальмує їх виділення. Введення соматос Гатіна в мозок тягне за собою зниження рухової активності і індукцію сну.
нейропептид Y (NPY) Включає в себе 36 амінокислот. Це один з найбільш представлених в периферичної НС і ЦНС пептид. Особливо багато цього пептиду в вегетативних гангліях, иннервирующих серцево судинну систему, де і була показана його медіаторная роль в організмі. Відомо про співіснування в одних закінченнях NPY і НА. При введенні в мозок NPY індукує піщедобивательное поведінку, знижує рухову активність, зменшує тривожність.
опіоїдні пептиди в літературі часто називають ендогенними пептидними анальгетиками (ЕПА). Відкриття системи пептидних регуляторів почалося з виявлення ЕПА - лігандів рецепторів до морфіну.
Природно, що нейрохімікі шукали в мозку та інших органах рецептори, з якими зв'язуються введені в організм опіоїди. І ось в 1970-і рр. такі рецептори були виділені, а потім, ще через кілька років, були знайдені ті речовини в організмі, які з цими рецепторами пов'язуються. Вони виявилися невеликими пептидами, які тепер відносять до трьох класів: енкефаліни (5 амінокислот), ендорфіни (31 амінокислота), динорфінів (17 амінокислот). Насправді до складу кожного класу входить по кілька пептидів. Всі ці пептиди, як і взагалі РП, утворюються в мозку з набагато більш довгих молекул-попередників: нроенкефаліна, іродінорфіна, іроопіомеланокортіна. В останні роки відкриті нові опіоїдні пептиди, найцікавіші з яких - ендоморфінів, що складаються всього з чотирьох амінокислот і по своїй просторовій структурі нагадують морфін, а також Ноціцептін, що складається з 17 амінокислот (хоча активність проявляють і його короткі фрагменти). Ноціцептін, взаємодіючи з рецепторами до опіатів, на відміну від інших подібних з'єднань, підсилює відчуття болю.
З огляду на, що в організмі був виявлений не один, а кілька різних лігандів до опіатних рецепторів, не було несподіванкою виділення декількох різновидів опіатнихрецепторів. В даний час відомо чотири типи рецепторів: р- (мю), до- (каппа), 8- (дельта) і ORL-1, причому у більшості з них є підтипи. Всі опіатні рецептори є метаботропнимі (див. Рис. 9.7). Ліганд взаємодіє з зовнішньою частиною рецептора, запускаючи каскад рецепторних реакцій. Первинна структура молекул різних рецепторів подібна приблизно на 70%. Рецептор пов'язаний з Gf і С ^ -белкамі. При зв'язуванні з рецептором природного опиоида штучного агоніста гальмується АЦ, зменшується синтез цАМФ і відкриваються К ~ -канали (р-, 8- і ORL-1 - рецептори) або блокуються Са2+-канали (к-рецептор) і вивільнення медіаторів цією клітиною порушується. Залежно від того, на яких нейронах розташовані опіатні рецептори, ця блокада поширюється і на збуджуючі, і на гальмівні системи.
Найчастіше пептідергічні закінчення розташовуються пресинаптичними, т. Е. На синаптичних закінченнях інших нейронів. Опіоїдні рецептори представлені в мозку дуже широко. Вони знайдені як на тілах, так і на відростках нейронів в корі великих півкуль, хвостатому ядрі, перегородці, таламусі, гіпоталамусі. Області мозку, в яких знайдені рецептори до опіатів, перекриваються між собою і з областями, де представлені рецептори інших медіаторних систем, зокрема дофамінер- ня. Крім того, опіоїдні рецептори виявлені і в периферичних нервових утвореннях, а також в інших органах (в серці, кишечнику та ін.). Деякі фізіологічні ефекти ЕПА наведені в табл. 10.1. У таблиці і на рис. 10.4 вказана основна спрямованість ефектів опіатів без урахування способу введення і використовуваних доз.
Таблиця 10.1
Фізіологічні ефекти ЕПА
|
РП |
мет ен кефалі ни лей енкефаліни |
р-Ендор- фін |
Дінор- фіни |
ендоморфінів |
|
|
рецептори |
5, ц |
до |
М |
||
|
деякі фізіологічні ефекти |
анальгезия |
+ |
++ |
+ |
+++ |
|
Ейфорія і залежність |
+ |
++ |
++ |
||
|
седативний ефект |
- |
+ |
+ |
+ |
|
|
РП |
мет енкефаліни лей енкефаліни |
[З-Ендор- фін |
Дінор- фіни |
Ендомор фіни |
|
|
рецептори |
5, р |
М. § |
до |
м |
|
|
пригнічення дихання |
+ |
+ + |
+ |
++ |
|
|
Посилення тонусу гладкої мускулатури |
+ |
+ |
+ |
+ |
|
|
Зниження температури тіла |
+ |
+ |
+ |
||
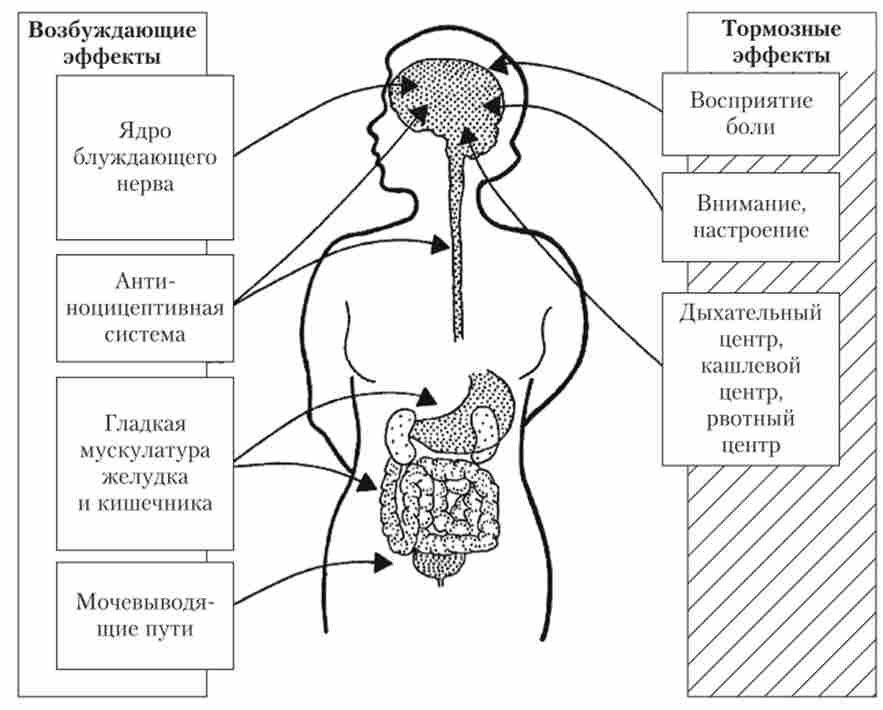
Мал. 10.4. Основні ефекти ендогенних оніоідних пептидів
Вплив ЕІ А і їх синтетичних агоністів і антагоністів на організм складно і вариабельно, а головне, супроводжується виникненням толерантності та розвитком фізичної і психічної залежності. Все це, здавалося б, вказує на неможливість застосування такого роду препаратів в клінічній практиці. Однак аналоги р-опіатних рецепторів є неперевершеними анальгетиками, і їх вводять хворим не тільки з почуття жалю, а й для того, щоб уникнути больового шоку.
Наркотичні анальгетики, що діють через систему опіатнихрецепторів, призначають при станах, що супроводжуються гострим болем. Найчастіше це опіки, травматичні ушкодження, інфаркти міокарда, запалення очеревини (перитоніт), ниркова колька і ін. При спазмах гладкої мускулатури наркотичні анальгетики призначають разом з блокаторами мускаринових холінорецепторів. При хронічних захворюваннях наркотичні анальгетики застосовувати не можна через виникнення залежності. Єдиний виняток - онкологічні захворювання, коли хворий страждає від сильного болю. Знеболюючі препарати слід вводити до розвитку нестерпних болів, в цьому випадку подіють менші дози ліків. У клініці застосовують: про- Медоле, трамадол, бупренорфін, налбуфин, буторфанол, пентазоцин та ін.
Наркотичні анальгетики треба вживати з обережністю, оскільки їх передозування може призвести до зупинки дихального центру.
Призначення більшості опадів регулюється певними правилами. Деякі опіоїдні анальгетики (кодеїн і трамадол) можуть виписуватися в звичайному порядку, так як ризик виникнення залежності від цих препаратів невеликий.
Різниця в активності опадів і їх здатності викликати залежність обумовлено спорідненістю до різних типів рецепторів. Речовина не може діяти однаково на всі типи рецепторів: по відношенню до одного типу рецепторів воно - агоніст, до іншого - антагоніст або частковий агоніст / антагоніст.
Механізм анальгетичної (антіпоціцептівного) дії ЕПА здійснюється на декількох рівнях і не до кінця вивчений. Відомо, однак, що опіатергічні нейрони утворюють пресинаптичні закінчення на міжклітинних контактах між рецепторними клітинами, що сприймають біль, і нейронами задніх рогів СМ, які повинні проводити інформацію про болі в ГМ. Виділяються ЕПА знижують в «больовому» синаптичному закінчення активність АЦ, а отже, і синтез цАМФ. Крім того, ЕПА сприяють відкриттю До+-каналів і зменшення надходження Са2+ до клітки. Все це призводить до гіперполяризації закінчення і блокаді викиду з його везикул медіаторів больових шляхів SP і глутамату. В результаті больовий сигнал послаблюється або блокується (рис. 10.5).
Крім того, ЕПА діє на рівні структур стовбура мозку, стимулюючи (шляхом гальмування ГАМК-ергічних впливів) норадренергичні і серотонііергічні нейрони, аксони яких йдуть в СМ і теж пригнічують активність нейронів спино-таламичного тракту, що призводять больову інформацію.
ЕПА також впливають на суб'єктивну оцінку і сприйняття болю людиною. Гальмуючи активність центрів емоційності (лімбічна система, гіпоталамус, кора великих півкуль), оііоіди послаблюють негативну емоційну оцінку болю, і хворі, відчуваючи біль, відносяться до неї байдуже, без страждань і страху. Можливо, одна з причин цього ефекту полягає в тому, що агоністи р-рецепторів, в тому числі і морфін, викликають підвищене виділення в корі, стриатуме, лімбічної системи і гіпоталамусі такого важливого фактора внутрішнього підкріплення, як Д.
У цьому розділі ми говоримо головним чином про тих регуляторних пептидах, які є медіаторами. В даний час відомо, як уже говорилося, не менше 1000 пептидів, рознесених приблизно
по 50 класам. Про багатьох пептидах ще буде сказано в інших розділах цього підручника.
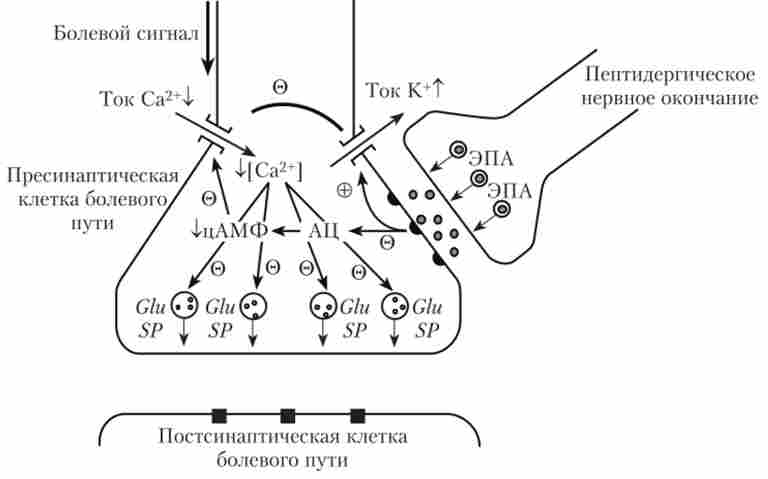
Мал. 10.5. Блокада проведення больовий інформації (медіатори - глутамат (Glu) І субстанція Р (SP)) Ендогенними пептидними анальгетиками (ЕПА)