
| Головна |
| «« | ЗМІСТ | »» |
|---|
Відомо більше 2000 різних реакцій, що каталізуються ферментами. Міжнародним союзом по біохімії (International Union of Biochemisry, IUB) створена і рекомендована до повсюдного використання систематика ферментів, що дозволяє орієнтуватися в цій множині біохімічних з'єднань.
Всі ферменти включені в «Каталог ферментів» під своїм класифікаційним номером (КФ), що складається з чотирьох цифр. В рамках цієї класифікації ферменти поділені на шість класів.
Вони класифікуються не як індивідуальні речовини, а як каталізатори певних хімічних перетворень або груп хімічних перетворень. Ферменти, виділені з різних біологічних джерел і каталізують ідентичні реакції, можуть досить істотно відрізнятися за своєю первинну структуру, проте всі вони в класифікації мають однаковий шифр.
Перша цифра шифру вказує на приналежність до одного з шести головних класів. Наступні дві визначають підклас і подподкласса, а остання - номер ферменту в даному подподкласса. наприклад, лактатдегидрогеназа має номер КФ 1.1.1.27 (клас 1 - оксидоредуктаз; підклас 1.1 - донор електрона (група - СН-ОН); подподкласса 1.1.1 (акцептор - NAD *).
В даний час прийняті два типи назв ферментів: робоче, або тривіальне, і систематичне. Робоча є назва субстрату, типу каталізуються реакції і закінчення -аза.
наприклад:

Лактат + дегідрогенізація (процес відщеплення Нч) + - аза = лактатдегидрогеназа.
Залишені робочі (тривіальні) назви для ряду давно відомих ферментів: пепсин, трипсин, хімотрипсин і т.д.
Систематичне назва ферменту утворюється складніше. Воно складається з назв субстратів хімічної реакції, на які діє фермент, назви типу катализируемого хімічного перетворення і закінчення -аза.
Наприклад, систематичне назва ферменту лактатдегідрогенази пишеться так:
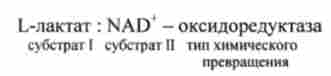
Як сказано вище, все ферменти розділені на шість класів, в кожному з яких об'єднані ферменти, що володіють однаковою реакційної специфічністю.
До 1-го класу оксидоредуктаз відносяться практично всі ферменти, що каталізують окислювально-відновні перетворення.
Оксидоредуктази поділяються на 17 підкласів. Субстрат, що піддається окисленню Оксидоредуктази, розглядається як донор водню. Тому ферменти цього класу називають дегідрогеназ або, рідше, редуктази. Їх систематичне назва складається з назви відновника (донора електронів), окислювача (акцептора електронів) і назви класу.
Наприклад, фермент, що каталізує окислення етанолу до ацетальдегіду з використанням NAD * в якості окислювача, за систематичною номенклатурою називається алкоголь: NAD+ - оксидоредуктаза (шифр 1.1.1):
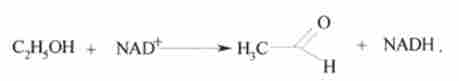
Підкласи оксидоредуктаз здебільшого визначаються типами з'єднань, які виступають в якості донорів електронів.
Ферменти, що каталізують окислення:
і діючі:
В окремі підкласи виділені ферменти (оксигенази), каталізують реакції введення в окислюються речовина одного атома кисню - підклас 14 (монооксигенази) або двох атомів кисню - підклас 13 (діоксигенази).
До 2-го класу трансферти відносять ферменти, які каталізують реакції перенесення різних груп від одного субстрату (донор) до іншого (акцептор), які не є гідролізом. Грансферази поділяються на 8 підкласів залежно від будови їх переносите ними груп. Ферменти, що каталізують перенесення метильних груп, називають метілтрансферазамн, амінних - амінотрансфе- разами і т. Д. В принципі, до трансферазу можна віднести і оксидоредуктаз, якщо вважати головним не процес окислення-відновлення, а перенесення групи від донора до акцептора, що супроводжується окісленіем- відновленням. Ці ферменти можна назвати протонтрансферазамі, електронтрансферазамі і т. Д.
Ферменти, що каталізують реакції перенесення:
ацетил-КоА (в латинському написанні СоА), що містить групу, що підлягає перенесенню, наприклад:
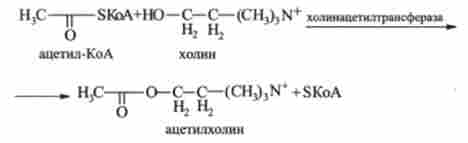
Ферменти 3-го класу - гідролізу - каталізують різні реакції гідролізу. Гідролази поділяються на 11 підкласів. Тривіальне їх назва утворюється шляхом приєднання до назви субстрату закінчення -аза. Систематичне назва обов'язково містить термін «гідролаза». В принципі, вони також можуть бути віднесені до трансферазу, оскільки гідроліз можна розглядати як перенесення специфічної групи субстрату, що є донором, на молекулу води, яка є акцептором. Однак роль води як акцептора вважається головною в дію цих ферментів, тому дані ферменти виділені в окремий клас гидролаз.
наприклад:
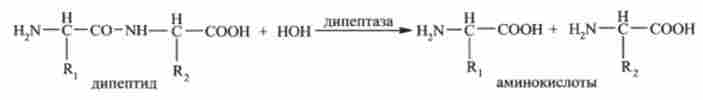
Підкласи виділяють відповідно до типу гідролізуемих зв'язків. Ферменти, що каталізують гідроліз:
Наприклад, каталізатор форміл-КоА-гідролаза (шифр 3.1.2):

Функцією більшого числа гідролаз є гідроліз біополімерів - білків, нуклеїнових кислот, полісахаридів. В основному це травні ферменти, наприклад пепсин - протеаза, що розщеплює білки на великі фрагменти.
Ферменти 4-го класу, ліази, в одному напрямку каталізують негідролітічним розщеплення субстрату з утворенням кратного зв'язку, а в іншому - приєднання кратного зв'язку.
наприклад:

При розриві зв'язку С-О виникає друга кратна зв'язок і утворюється молекула СО2 (фермент карбоан гід рази, шифр 4.2.1):
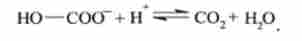
Ліази поділяються на чотири підкласу і класифікуються за типом розривається зв'язку:
Систематичне назва складається за принципом субстрат-група-ЛіАЗ. У тривіальних назвах ЛіАЗ вказується особливість участі груп в реакціях - карбоксилаза (приєднання карбоксильної групи), дегідратази (відібрання молекули води від субстрату).
Якщо необхідно підкреслити освіту субстрату з двох субстратів більш простого будови, то в назві ЛіАЗ вживається термін «синтаза», наприклад цитрат інтаза.
До 5-го класу відносять ізомерази - ферменти, що каталізують перетворення в межах однієї молекули, іншими словами, що каталізують різні процеси ізомеризації.
Ізомерази поділяються на п'ять підкласів. Назви ферментів складаються в залежності від типу реакції ізомеризації: мутази, таутомерази, раце- МАЗи. епімерази, ізомерази.
До підкласу 1 відносяться різні ферменти, за допомогою яких здійснюється звернення конфігурації при асиметричному атомі С:
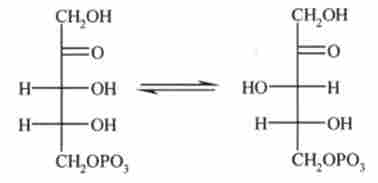
(Каталізатором є 0-рибулозо-5-фосфат-3-епімерази, шифр 5.1.3);
до підкласу 2 - ферменти, що каталізують цис-транс-ізомеризації;
до підкласу 3 - каталізують внутрішньо-молекулярні процеси окислення- відновлення (взаємоперетворенням апьдегоз і кетоз);
до підкласу 4 - каталізують внутрішньомолекулярне перенесення різних фрагментів і т. д.
У 6-й клас об'єднані лігази (Синтетази), що каталізують реакції конденсації або приєднання, пов'язані з гідролізом і використанням енергії фосфатного зв'язку.
Джерелом енергії в реакціях, що каталізуються синтетазами, є АТР (АТФ) або інші нуклеозидтрифосфат.
наприклад:
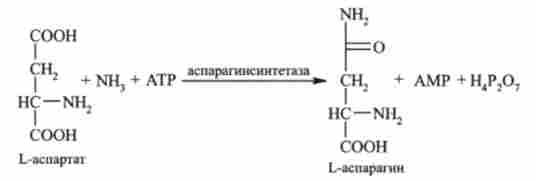
Поділ лигаз на підкласи пов'язано з типом утвореною зв'язку. Це ферменти, що каталізують утворення зв'язків
Наприклад, в реакції
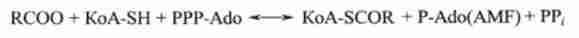
каталізатор - ацил-КоА-синтетаза (6.2.1).